Биохимические закономерности восстановления после мышечной работы
Тест
1. Субстраты, израсходованные во время
работы, восстанавливаются в
последовательности:
а)
белки, жиры, креатинфосфат
б)
жиры, креатинфосфат, белки
в)
креатинфосфат, гликоген, жиры
г)
гликоген, жиры, креатинфосфат
Тест
2.
Максимальное
время восстановления запасов гликогена
мышцах после работы большого объема:
а)
20-30 с.
б)
4-5 мин.
в)
18-24 час.
г)
2-3 суток
Тест
3. Максимальное время устранения лактата
после выполнения лактатных нагрузок:
а)
20-30 с
б)
4-5 мин.
в)
60-90 мин.
г)
2-3 суток
Тест
4. После тренировки быстрей всего
восстанавливаются запасы:
а)
белков
б)
гликогена
в)
жиров
г)
креатинфосфата
Тест
5. Максимальное время восстановления
запасов креатинфосфата в мышцах после
выполнения алактатных нагрузок:
а)
20-30 с
б)
4-5 мин.
в)
18-24 час.
г)
2-3 суток
Тест
6. Отставленное восстановление направлено
на восполнение в мышцах запасов:
а)
гликогена
б)
ионов кальция
в)
креатинфосфата
г)
миоглобина
Тест
7. Быстрое исчерпание запасов
креатинфосфата в мышцах наблюдается
при выполнении нагрузок в зоне:
а)
максимальной мощности
б)
субмаксимальной мощности
в)
большой мощности
г)
умеренной мощности
Тест
8. Максимальное время восстановления
запасов белков в мышцах после
продолжительной работы силового
характера:
а)
4-5 мин.
б)
18-24 час.
в)
2-3 суток
г)
7-8 суток
Тест
9. Синтез гликогена ускоряет гормон:
а)
адреналин
б)
инсулин
в)
кортикостерон
г)
тестостерон
Тест
10. Синтез мышечных белков ускоряет
гормон:
а)
адреналин
б)
кортикостерон
в)
тестостерон
г)
тироксин
Биохимические закономерности адаптации к мышечной работе
Тест
1. Биохимические сдвиги, лежащие в основе
срочной адаптации, преимущественно
вызываются гормоном:
а)
адреналином
б)
альдостероном
в)
кальцитонином
г)
тестостероном
Тест
2. Срочный тренировочный эффект – это
биохимические сдвиги в организме,
наблюдаемые:
а)
во время работы и в течение 1-2 час. после
ее завершения
б)
через 5-6 час. после работы
в)
через 2-3 суток после работы
г)
после многих лет занятий спортом
Тест
3.
Повышенное
потребление кислорода
во время мышечной работы является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
4. Кумулятивный тренировочный эффект –
это биохимические сдвиги в организме,
наблюдаемые:
а)
во время работы и в течение 1-2 час.
после ее завершения
б)
через 5-6 час. после работы
в)
через 2-3 суток после работы
г)
после многих лет занятий спортом
Тест
5. Снижение рН крови, наблюдаемое во
время мышечной работы, является
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
6.
Отставленный
тренировочный эффект – это биохимические
сдвиги в организме, наблюдаемые:
а)
во время работы и в течение 1-2 час.
после ее завершения
б)
через 2-3 час. после работы
в)
через 2-3 суток после работы
г)
после многих лет занятий спортом
Тест
7. Гипергликемия, возникающая во время
мышечной работы является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
8. Биохимические сдвиги, лежащие в основе
срочной адаптации, вызываются
преимущественно:
а)
андрогенами
б)
катехоламинами
в)
соматотропином
г)
эстрогенами
Тест
9. Лактатный кислородный долг является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
10. Мышечная гипертрофия, развивающаяся
после многолетних тренировок,
является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
11. Алактатный кислородный долг является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
12. Суперкомпенсация, возникающая во
время восстановления, является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
13. Гиперкетонемия, наблюдаемая во время
мышечной работы, долг является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
14. Увеличение размера и количества
митохондрий в мышечных клетках после
многолетних
тренировок является:
а)
кумулятивным тренировочным эффектом
б)
отставленным тренировочным эффектом
в)
срочным тренировочным эффектом
Тест
15. Срочным тренировочным эффектом
является:
а)
мышечная гипертрофия
б)
предстартовая гипергликемия
в)
смещение мышечного спектра в сторону
преобладание красных волокон
г)
суперкомпенсация гликогена
Тест
16. Кумулятивным тренировочным эффектом
является:
а)
лактатный кислородный долг
б)
предстартовая гипергликемия
в)
смещение мышечного спектра в сторону
преобладания белых волокон
г)
суперкомпенсация гликогена
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
О.Н. Вербицкий,
кандидаты биологических наук Л.В. Скорик, Е.В. Мельниченко,
кандидат медицинских наук В.Н. Коновальчук,
мастер спорта СССР С. Г. Пушкарь
Симферопольский государственный университет
Ключевые слова: физическая нагрузка, метаболический ацидоз, гидрокарбонатсодержащая солевая смесь.
Ранее была показана перспективность использования в спортивной практике гидрокарбонат-содержащей солевой смеси [2].
В работе изучалось влияние гидрокарбонат-содержащей солевой смеси на фоне различных тренировочных нагрузок с целью коррекции кислотно-щелочного равновесия (КЩР) крови в период выполнения интенсивной мышечной деятельности.
Методика. Проведено обследование пловцов опытной и контрольной групп (мастеров спорта, кандидатов в мастера спорта и перворазрядников, n=16, возраст 16-18 лет). Спортсмены выполняли аэробно-анаэробный тест [2] на фоне значительных нагрузок (состояние компенсированного утомления) и на фоне больших нагрузок (состояние явного утомления) [8] до и после 10-дневного приема солевой смеси. Опытная группа получала солевую смесь из расчета 70,4 мг/кг [3]. Контрольная группа — «плацебо». Параметры КЩР исследовали по методу Аструпа и определяли рН, дефицит буферных оснований (BE) и парциальное давление углекислого газа (рСО2) [10]. Содержание лактата в крови определяли по методу Штрома [11]. Биохимические исследования проводили в исходном состоянии, на 3-й и 10-й мин после теста. Статистическую обработку результатов осуществляли по критерию Стьюдента [5].
Результаты и обсуждение. Как видно из таблицы, на фоне значительных нагрузок в контрольной группе на 3-й мин после теста параметры КЩР смещались в сторону метаболического ацидоза, при этом рСО2 уменьшалось на 33%. На 10-й мин после теста происходило достоверное восстановление уровней рН и BE, тогда как рСО2 оставалось на том же уровне. В опытной группе после приема солевой смеси на 3-й мин после теста происходило менее выраженное смещение рН и BE в сторону ацидоза, при этом pCO2 достоверно не отличалось от значений контрольной группы. На 10-й мин после теста происходило восстановление рСО2, тогда как значения рН и BE достоверно не отличались от значений контрольной группы. Концентрация лактата при нагрузках также достоверно не отличалась между группами.
Из представленных в таблице данных видно, что прием солевой смеси на фоне значительных нагрузок приводит к менее выраженному смещению рН и BE на 3-й мин после теста и восстановлению рСО2 на 10-й мин после теста.
На фоне больших нагрузок в контрольной группе на 3-й мин после теста рН и BE смещались в сторону метаболического ацидоза и рСО2 уменьшалось на 43%. На 10-й мин после теста происходило дальнейшее смещение рН и BE в сторону ацидоза, при этом рСО2 снижалось на 79%. Концентрация лактата после теста на 3-й мин возрастала в 2,5 раза, а на 10-й мин оставалась на том же уровне. Отсутствие корреляционной зависимости между накоплением лактата и смещением КЩР в сторону метаболического ацидоза, вероятно, свидетельствует об истощении буферных систем крови. В опытной группе после приема солевой смеси, на 3-й мин после теста,
Влияние солевой смеси на показатели кислотно-щелочного равновесия и лактата крови после выполнения аэробно-анаэробного теста на фоне различных тренировочных нагрузок (М ±m, n=7-9)
| Показатели | фон тренировочной нагрузки | |||
| Значительная | Большая | |||
| контрольная группа (n=7) | опитная группа (n=9) | контрольная группа (n=7) | опытная группа (n=9) | |
| Исходное состояние | ||||
| pH | 7,41 ±0,01 | 7,43 ±0,01 | 7,39 ±0,01 | 7,44 ± 0,01* |
| BE, мэкв/л | 2,2±0,4 | 3,2±0,6 | -0,2±0,8 | 2,0 ±0,5 |
| рСО2, кПа | 5,77±0,11 | 5,68±0,26 | 5,57±0,32 | 5,01 ±0,21 |
| Лактат, мМоль | 2,8 ±0,3 | 3,5 ±0,3 | 2,6 ±0,3 | 2.7±0,2 |
| На 3-й мин после теста | ||||
| рН | 7,22±0,01 | 7,29 ±0,02* | 7,30 ±0.01 | 7,35±0,01* |
| BE, мэкв/л | -15,2±0,8 | -8,8 ±1,4* | -11,1±1,3 | -8,0±0,5* |
| рСО2, кПа | 4,44 ±0,50 | 4,26 ±0,26 | 3,80 ±0,29 | 3,86±0,32 |
| Лактат, мМоль |
8,5 ±0,7 |
8,7±0,5 | 6,4±1,1 | 9,2±1,3* |
| На 10-й мин после теста | ||||
| pH | 7,35±0,02 | 7,35 ± 0,02 | 7,2±0,03 | 7,38±0,01* |
| BE, мэкв/л | -5,2±1,0 | -4,3±1,6 | -16,0±1,3 | -4,3±0,6* |
| рСО2, кПа | 4,32±0,17 | 5,12±0,13* | 3,11± 0,33 | 4,26 ±0,25* |
| Лактат, мМоль |
6,5±0,4 |
6,0±0,5 | 6,7±0,8 |
6,3±0,7 |
* достоверные различия между опытной и контрольной группами, р <= 0,05
происходило менее выраженное смешение рН и BE в сторону ацидоза, при этом pCO2 достоверно не отличалось от значений контрольной группы. Концентрация лактата на 3-й мин после теста возрастала в 3,4 раза. Сравнение этих данных с показателями контрольной группы на 3-й мин после теста обнаружило менее выраженное смешение рН и BE в сторону ацидотического состояния при значительном (на 38%) повышении уровня лактата в крови. Способность организма переносить концентрацию лактата при меньших сдвигах КЩР в сторону ацидоза свидетельствует об увеличении емкости буферных систем крови, что позволяет выполнять больший объем работы [4]. На 10-й мин после теста происходило достоверное восстановление показателей КЩР. Концентрация лактата уменьшалась на 43%. Более быстрое уменьшение лактата в крови после интенсивной физической нагрузки служит результирующим показателем ускорения процессов восстановления в организме спортсменов [1].
Полученные данные свидетельствуют, что применение гидрокарбонатсодержащей солевой смеси на фоне больших нагрузок не только уменьшает степень ацидоза, но и предотвращает истощение буферных систем крови.
Определенный интерес представляет возможность регуляции уровня pCO2 в крови в период выполнения интенсивных физических нагрузок. Известно, что уменьшение pCO2 в крови говорит о постепенном истощении запасов гидрокарбонатов [6]. По мере увеличения функциональных возможностей организма степень снижения рСО2 уменьшается [9]. Более быстрое восстановление уровня рСО2 после приема солевой смеси на фоне значительных нагрузок препятствует истощению запасов гидрокарбоната и создает благоприятное условие для биосинтетических процессов в организме спортсменов [7].
Как видно из таблицы, смещение BE в сторону ацидоза после выполнения аэробно-анаэробного теста на фоне значительных и больших нагрузок различно по времени возникновения: при больших нагрузках ацидоз развивается медленнее. Так. величина сдвига BE на 3-й и 10-й мин после теста в результате приема солевой смеси уменьшается соответственно в 1,9 и 3,7 раза.
Таким образом, в вопросе о назначении приема гидрокарбонатсодержащей солевой смеси важен учет максимальной величины сдвига BE во времени.
Литература
1. Бродан В., Кун Э. «Чехословац. мед. обозрение», 1971, вып. 17, № 2, с. 93-120.
2. Вербицкий О.Н., Толкачева Н.В., Мельничук Д.А. «Укр. биохим. журн.», 1984, вып. 56, № 1, с. 94-96.
3. Гулый М.Ф., Мельничук Д.А. «Успехи биол. химии», 1980, № 21, с. 185-208.
4. Калинин В.М. «Теор. и практ. физ. культ.», 1981, № 12, с. 17-18.
5. Кокуин В.А. «Укр. биохим. журн.», 1975, вып. 47, № 6, с. 776.
6. Красников Н.П. «Физиол. журн.», 1987, вып. 33, № 3, с. 18-24.
7. Мельничук Д.А. «Укр. биохим. журн.», 1989, вып. 61, № 3, с. 3-21.
8. Платонов В.Н., Вайцеховский С.М. Тренировка пловцов высокого класса. — М.: ФиС, 1985.
9. Филиппов М.М., Миняйленко Т.Д. «Укр. биохим. журн.», 1980, вып. 52, № 2, с. 171-174.
10. Astrup et al. «Lancet», 1960, v. 1, No 7131, p. 1035.
11. Strom G. «Acta physiol. Scand.», 1949, No 17, s. 440.
Поступила в редакцию 31.05.93
Дано определение водородного показателя (рН). Приведены значения рН крови, мочи и саркоплазмы мышечных волокон у здоровых людей не занимающихся физической культурой и спортом и спортсменов. Дано определение ацидоза.
рН крови, мочи и саркоплазмы мышечных волокон
Определение
Водородный показатель, рН (от лат. pondus Hydrogeni – вес водорода) – мера кислотности водных растворов.
рН равен отрицательному десятичному логарифму[1] концентрации ионов водорода в среде: рН = –lg[H+].
В нейтральной среде рН равен 7 (рН=7). Например, водородный показатель чистой воды при 25 град равен 7,0 (рН=7).
Значение водородного показателя (рН) в кислой среде меньше 7 (рН<7). Чем меньше рН, тем выше кислотность среды. Например, значение водородного показателя (рН) лимонного сока равно 2,2 (рН=2,2).
В щелочной среде значение водородного показателя (рН) больше 7 (рН>7). Например, рН нашатырного спирта равен 11,5 (рН=11,5).
рН крови
В покое у здорового человека кровь имеет слабощелочную реакцию. Значение pH капиллярной крови (взятой из пальца руки) приблизительно равно 7,4 (рН=7,4); pH венозной крови равно 7,36 (рН=7,36).
Ацидоз
Ацидоз – повышение кислотности внутренней среды организма, связанное с накоплением в тканях кислых продуктов обмена веществ (Н.И. Волков с соав., 2000).
Ацидоз крови – повышение кислотности крови, обусловленное накоплением органических кислот, которые в дальнейшем подвергаются диссоциации. При этом выделяются ионы водорода. Поэтому кислотность крови повышается, а величина водородного показателя снижается. При ацидозе значение pH крови может уменьшаться до 7,0-6,8. Считается, что снижение pH крови ниже 6,8 несовместимо с жизнью (С.С. Михайлов, 2009).
рН мочи
У здорового человека значение водородного показателя во многом зависит от характера питания. При смешанном питании моча обычно имеет слабокислую реакцию, ее pH равен 5,5-6,5. Употребление преимущественно мясной пищи уменьшает значение водородного показателя. Он становится меньше 5. Наоборот, употребление растительной пищи приводит к увеличению водородного показателя, и pH может быть больше 7.
После интенсивных физических нагрузок кислотность мочи повышается (pH становится равным 4-5).
рН саркоплазмы мышечных волокон
В норме значение водородного показателя саркоплазмы мышечных волокон равно 7,1 (рН=7,1). После интенсивных физических нагрузок рН может понизиться до 6,5. Это происходит потому, что в саркоплазме активно протекают два процесса, вызывающие увеличение концентрации ионов водорода: гидролиз АТФ и гликолиз.
Долгое время считалось, что именно анаэробный гликолиз, приводящий к накоплению в мышечных волокнах молочной кислоты является основной причиной их ацидоза («закисления»). Однако в настоящее время доказано (R.A. Robergs, 2001) что реакция гидролиза АТФ, а не гликолиза является основным поставщиком ионов водорода в саркоплазму мышечных волокон и причиной снижения рН с 7,1 до 6,5. Гликолиз также поставляет в мышечные волокна ионы водорода, но в меньшей степени. В результате «закисления» мышц спортсмены испытывают на тренировке боль и жжение.
Видео про рН саркоплазмы
Литература
- Волков Н.И. Биохимия мышечной деятельности / Н.И.Волков, Э.Н.Несен, А.А.Осипенко, С.Н. Корзун.– Киев: Олимпийская литература, 2000.– 503 с.
- Михайлов С.С. Спортивная биохимия: учебник для вузов и колледжей физической культуры.– М: Советский спорт, 2009.– 348 с.
- Robergs RA. Exercise-induced metabolic acidosis: where do the protons come from? // Sportscience 5. [sportsci.org/jour/0102/rar. htm, 2001].
С уважением, А.В. Самсонова
[1] Логарифмом числа b по основанию a называется показатель степени, в которую нужно возвести a чтобы получить число b. Обозначается:
Например,
У десятичных логарифмов (обозначаются lg) основание a равно 10. Поэтому запись lg100=2, означает 102=100.
Если lgb = –2, это означает, что 10-2= 0,01, то есть число b=0,01.
Если –lgb=7, это означает, что число 10 должно быть в степени –7, то есть
10-7=0,0000001.
Если –lg[H+]=7. Это означает, что [H+]=10–7=0,0000001 – такая концентрация ионов водорода в нейтральной среде
Если –lg[H+]=6. Это означает, что [H+]=10–6=0,000001, то есть концентрация ионов водорода повышается.
Если –lg[H+]=8. Это означает, что [H+]=10–8=0,00000001, то есть концентрация ионов водорода понижается.
Следовательно сдвиг рН на одну единицу соответствует изменению концентрации ионов водорода в 10 раз.
Похожие записи:
Типы конституции женщин по И.Б. Галанту
Дана биография известного советского психиатра И.Б.Галанта. Описаны типы конституции женщин по И.Б. Галанту: астенический, стенопластический, пикнический, мезопластический, атлетический,…
Сила тяжести
Дано определение силы тяжести. Показано, что сила тяжести является частным случаем силы гравитации. Описаны факторы, определяющие силу тяжести:…
Сила
Дано определение силы в механике. Описаны факторы, определяющие действие на тело силы: направление, точка приложения и численное значение.
Физиология и нарушения кислотно-основного состояния (методические материалы к практическим и семинарским занятиям)
Категория:
КазМУНО (АГИУВ). Кафедра анестезиологии и реаниматологии
Информация
Физиология и нарушения кислотно-основного состояния
Методические материалы к практическим и семинарским занятиям
Физиология и нарушения кислотно-основного состояния. Методические материалы к практическим и семинарским занятиям, – 2011. -21 с.
Составители: к.м.н. Батырханова Н.М., ассистент Прмагамбетов Г.К., резидент Иманбекова К.Б., резидент Тлеубаев С.С., под редакцией доцента Чурсина В.В.
Справочное пособие содержит информацию о физиологии кислотно- основного состояния (КОС). Представлена информация о методах лабораторной диагностики нарушений КОС. Перечислены варианты нарушений и методы коррекции. Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
© Чурсин В.В., Батырханова Н.М., Прмагамбетов Г.К., Иманбекова К.Б., Тлеубаев С.С., 2011 г.
Физиология кислотно-основного состояния
В результате жизнедеятельности клетки в ней постоянно образуются кислоты, которые диссоциируют с освобождением очень активных ионов Н+. Часть этих ионов нейтрализуется буферной системной клетки, другая — буферными системами межклеточной жидкости и крови, а также при функционировании легких, почек, кишечника, печени и др.
Соотношение водородных и гидроксильных ионов во внутренней среде в значительной мере определяет интенсивность окислительно-восстановительных процессов, синтез и расщепление белков, жиров и углеводов, активность ферментов, проницаемость мембран, чувствительность к гормональным стимулам и др. Это соотношение выражается в интегральном показателе рН. Учитывая, что показатель рН часто встречается в медицинской литературе, мы дадим ему более подробную характеристику. Кислотность или щелочность раствора зависит от содержания в нем свободных ионов водорода и концентрации гидроксильных групп.
Если концентрация Н+ > концентрации ОН— — рН кислая
Если концентрация Н+ = концентрации ОН— — рН нейтральная
Если концентрация Н+ < концентрации ОН— — рН щелочная
Эталон нормы – концентрация Н+ = 0,00000001 моль/л в 1 литре химически чистой воды при t0 250С. При этом рН будет нейтральной. Для удобства используют коэффициент рН. Термин «рН» представляет собой аббревиатуру от слов «puissance hydrogen» (puissance по-французски означает сила). Это мера активности или концентрации ионов водорода. рН определяют как отрицательный десятичный логарифм концентрации ионов водорода в моль/л:
pH=-Ig [H+] (конц. Н+) = 7,0
Из этого уравнения следует, что:
рН <7,0 — кислая среда
рН =7,0- нейтральная среда
рН >7,0 – щелочная среда
Для адекватного клеточного метаболизма требуется, чтобы уровень рН крови сохранялся в границах 7,35-7,45, несмотря на постоянную продукцию ионов водорода, которые понижают рН. Даже незначительные нарушения этих границ рН могут иметь неприятные последствия, а снижение рН менее 6,8 и повышение до 7,8 несовместимы с жизнью.
В некоторых случаях лаборатории предпочитают использовать показатель концентрации ионов водорода в нмоль/л, а не рН.
рН 7,4 = концентрация ионов водорода 40 нмоль/л;
рН 7,0 = концентрация ионов водорода 100 нмоль/л;
рН 6,0 = концентрация ионов водорода 1000 нмоль/л.
■ два этих параметра (рН и концентрация Н+) изменяются в противоположных направлениях — если концентрация ионов водорода возрастает, то рН снижается;
■ благодаря логарифмической природе шкалы незначительные изменения рН означают фактически очень существенные изменения концентрации ионов водорода. Например, удвоение концентрации ионов водорода соответствует снижению рН всего на 0,3 единицы.
Факторы, определяющие постоянство рН:
— продукция Н+ за счет катаболизма кислот
— дальнейшее преобразование и распределение кислот в организме
— выведение Н+ из организма
Продукция Н+ происходит в результате расщепления белков, жиров и углеводов. У взрослого человека за сутки вырабатывается 20000 — 22000 ммоль Н+. При перерасчете на НС1 это составит 2 -2,5 л.
В организме продуцируется два вида кислот:
— Н2С03 угольная кислота — летучая кислота, которая выводится через легкие — (слабая кислота, т.к. плохо диссоциирует),
— нелетучие кислоты – H3P04 и Н2SО4 — не выводятся через легкие, но выводятся почками (сильные кислоты, т.к. хорошо диссоциируют).
В норме сильных кислот образуется 50 – 100 ммоль/сутки. При избыточном образовании они вызывают тяжелые нарушения. Это происходит при анаэробном окислении глюкозы.
В норме окисление глюкозы происходит аэробно: С6Н12О2 + 6О2 = 6Н2О + 6СО2 + 38 АТФ
При патологии глюкоза окисляется анаэробно: С6Н12О2 = 2СН2 + 2СН(ОН)СООН + 2 АТФ
В результате образуется избыток кислот и дефицит энергии.
Преобразование и распределение кислот в организме происходит за счет:
-разведения (пассивного механизма);
-действия буферных систем.
Чтобы понять принцип работы химических буферных систем необходимо
разобрать:
Что такое кислоты и основания?
Кислота — это вещество, которое диссоциирует в растворе с высвобождением ионов водорода. Основания (щелочи) присоединяют ионы водорода.
Например, соляная кислота (НС1) диссоциирует на ионы водорода и ионы хлора:
НС1 ↔ Н++Сl—
тогда как бикарбонат (НС03), являющийся основанием, захватывает ион водорода, образуя угольную кислоту:
НСОз + Н+ ↔ Н2С03
Сильные кислоты, такие как соляная, диссоциируют легко, освобождая большое количество водородных ионов, т. е. они имеют очень низкое значение рН. Слабые кислоты диссоциируют хуже, поэтому высвобождается меньше ионов водорода, т. е. они имеют более высокие значения рН, чем сильные кислоты. Иными словами сила кислоты определяется способностью к диссоциации, т.е. степенью, с которой реакция смещается вправо. Водород проявляет кислотные свойства только в ионной форме.
Буферы — это растворы химических композиций, которые способны сглаживать изменения рН, вызываемые добавлением кислоты, при помощи нейтрализации образующихся ионов водорода. Буфер состоит из основания и какой-либо слабой кислоты. Попадание в плазму сильной кислоты вызывает реакцию буферных систем, в результате которой сильная кислота превращается в слабую. То же происходит и при действии на биологические жидкости сильного основания, которое после взаимодействия с буферными системами превращается в слабое основание. В результате указанных процессов изменения рН либо не наступают, либо бывают минимальными.
Бикарбонаты обеспечивают 53% буферной способности крови, небикарбонатные системы — 47%: гемоглобиновый буфер (35%), протеиновый (7%) и фосфатный (5%). Кровь составляет только 1/5 общей буферной ёмкости организма.
1. Бикарбонатная
2. Фосфатная
3. Гемоглобиновая
4. Белковая
Бикарбонатный буфер состоит из угольной кислоты и бикарбоната, в соотношении 1:20
Основная роль данного буфера это перевод сильной кислоты в слабую, сильного основания в слабое:
NаОН + H 2C03 ↔ NаHC03 + Н2О
НСl + NаHC03 ↔ Nа Сl+ H 2C03
↓
С02 + Н2О
Система утрачивает буферные свойства при рН= 6,1, когда соотношение H 2C03 / NаHC03 = 1 /1
Происхождение бикарбонатной буферной системы тесно связано с метаболизмом органического углерода, поскольку конечным продуктом его является СО2 или НСО3— .
Бикарбонатный буфер – главная и единственная система внеклеточной жидкости.
Участие бикарбонатного буфера в выведении H+:
Кислород из вдыхаемого воздуха диффундирует через альвеолы в легкие и соединяется с гемоглобином, который, проявляя буферные свойства, высвобождает ионы водорода:
Освободившиеся ионы водорода буферируются бикарбонатом с образованием угольной кислоты, которая превращается в углекислый газ и воду:
H+ + HC03 ↔ Н2СО3 ↔ С02 + Н2О
Углекислый газ диффундирует из крови в альвеолы и выводится из организма с выдыхаемым воздухом.
Фосфатная буферная система (1% буферной емкости крови) состоит из фосфорнокислых солей: кислотная часть представлена в виде однозамещенного фосфата натрия NaH2P04, а основная часть представлена двузамещенным фосфатом натрия — Na2HP04. Одноосновные фосфатные соли являются слабыми кислотами, а двухосновные соли имеют ясно выраженную щелочную реакцию.
NaH2P04 / Na2HP04 = 1/4 при рН=7,4
Принцип действия фосфатного буфера аналогичен карбонатному. Непосредственная роль фосфатного буфера в крови небольшая, но ему принадлежит значительная роль в конечной регуляции кислотно-основного гомеостаза и регуляции активной реакции тканей. В крови действие этого буфера сводится к поддержанию и воспроизводству бикарбонатного буфера.
При увеличении в крови кислот и образовании Н2С03 происходит обменная реакция:
H++HC03— + Na2HP04 = NaHC03 + NaH2P04
Избыток Н2С03 ликвидируется, а концентрация НС03 — увеличивается.
Таким образом, удерживается соотношение Н2С03/ NaHCO3= l:20 на постоянном уровне.
02НЬ – слабое основание
С02 – слабая кислота
Участие легких в кислотно-основном равновесии состоит в поддержании содержания углекислого газа (С02) в крови. Нормальное количество С02 в крови отражает равновесие между его продукцией в процессе клеточного обмена и выведением легкими с выдыхаемым воздухом. Последовательность событий от продукции С02 в тканях до его элиминации при выдохе выглядит следующим образом (рис. 1):
■ 1. С02 диффундирует из тканей (с высоким содержанием С02) в кровь.
■ 2.В эритроцитах крови С02 превращается в угольную кислоту при участии фермента карбоангидразы. Угольная кислота диссоциирует с образованием бикарбоната и ионов водорода:
С02+ Н20 ↔ Н2С03 ↔ НСО3 — + Н+
■ 3. Так как концентрация бикарбоната растет, часть его диффундирует из эритроцитов в плазму. Ионы водорода (которые, если позволить им накопиться, могут вызвать сильное снижение рН) связываются, с гемоглобином, который освобождается от принесенного кислорода в тканях (гемоглобин в данном случае действует как буфер).
Н+ + 02НЬ ↔ Н+НЬ + 02
■ 4. Когда кровь насыщена кислородом. Кислород из вдыхаемого воздуха диффундирует через альвеолы легких и соединяется с гемоглобином, который, проявляя буферные свойства, высвобождает ионы водорода.
02 + Н+НЬ ↔ Н+ + 02НЬ
■ 5. Освободившиеся ионы водорода буферируются бикарбонатом с образованием угольной кислоты, которая превращается в С02 и воду:
Н+ + НС03— ↔ H2C03 ↔ Н20 + С02
■ 6.С02 диффундирует из крови, где он находится в высокой концентрации, в альвеолы, где концентрация мала, и выводится из организма с выдыхаемым воздухом.
Рис. 1. Доставка 02 к тканям и первые стадии элиминации CO2
Рис. 2. В легких бикарбонат снова превращается в С02 и выводится
Транспорт кислорода из легких к тканям и из тканей к легким обусловлен изменениями, которые воздействуют на сродство кислорода к гемоглобину. На уровне тканей из-за снижения рН это сродство уменьшается (эффект Бора) и вследствие этого улучшается отдача кислорода. В крови легочных капилляров сродство гемоглобина к кислороду увеличивается из-за снижения рС02 и возрастания рН по сравнению с аналогичными показателями венозной крови, что приводит к повышению насыщения артериальной крови кислородом.
Белки плазмы крови – амфолиты – обладают свойствами кислот. Они составляют большую часть пула анионов плазмы. Изменение содержания альбуминов, протеинов и аномальных белков плазмы оказывает существенное влияние на величину анионной разницы.
Если в крови много Н+, то белки их связывают:
R-CООН + Н+→ R-CООН2
Если в крови много ОН—, то белки отдают Н+ и образуется вода:
R-CООН + ОН—→ R-CОО + Н2О
Выведение Н+ из организма
Почки
Нейтрализация и секреция ионов водорода происходит в результате их обмена с натрием в буферах первичной мочи. Бикарбонатные ионы, которые остаются после выхода Н+ в канальцевую мочу, реабсорбируются в кровь, повышая ее буферную способность. Процесс выведения эпителием почечных канальцев ионов Н+ происходит одновременно с реабсорбцией эквивалентного количества ионов Nа+.
При усиленном выделении почками кислот на уровне дистальных канальцев и собирательных трубок включается механизм аммониогенеза.
Аммиак (NН3) с одной стороны обеспечивает связывание Н+, с другой стороны – выведение анионов сильных кислот в виде аммонийных солей, в составе которых ионы Н+ не оказывают повреждающего действия на эпителий канальцев. Реабсорбция натрия происходит в обмен на выделение как ионов водорода, так и ионов калия. Этот обмен регулируется минералокорикоидами.
При недостатке ионов водорода может усилиться выделение калия, а при избытке – уменьшается.
Желудочно-кишечный тракт.
Клетки слизистой оболочки желудка секретируют Н+ и С1—, а в крови остаются Na+ и НС03—. Защелачивание крови не происходит, так как ионы хлора желудочного сока вновь всасываются в кишечнике. Эпителий слизистой оболочки кишечника секретирует щелочной сок Na+ и НСОз—. При этом в крови остаются Н+ и С1—. Кратковременный сдвиг реакции уравновешивается обратным всасыванием бикарбоната из кишечнике.
В то время, как почки концентрируют и выделяют из организма главным образом Н+ и одновалентные катионы, кишечный тракт концентрирует и выделяет двухвалентные щелочные ионы.
Участие печени
в нейтрализации кислот и оснований возможно за счет нескольких механизмов:
1) Органические кислоты, образующие в процессе метаболизма, в печени превращаются в межуточные и конечные продукты, которые не являются кислотами, или образуют углекислоту, быстро выделяющуюся из легких;
2) Некоторые органические кислоты нейтрализуются, образуя соединение с продуктами белкового обмена (соединение бензойной кислоты с гликогеном);
3) Молочная кислота нейтрализируется в печени, превращаясь в гликоген. Этот процесс имеет значение после усиления мышечной работы, когда в кровь поступает значительное количество молочной кислоты;
4) Неорганические кислоты задерживаются в печени, нейтрализуются и удаляются вместе с желчью. Также удаляются вместе с желчью и основания;
5) В печени происходит нейтрализация кислот аммиаком, образующимся при дезаминировании аминокислот и некоторых других продуктов белкового обмена.
Первичные изменения КЩС и компенсаторные реакции
Компенсаторные реакции немедленного типа
Дыхательная компенсация срабатывает при метаболических нарушениях (ацидоз, алкалоз).
Через легкие выводится в большей или меньшей степени С02. Это зависит от возбуждения или угнетения дыхательного центра.
Возбуждает дыхательный центр увеличение рС02 и снижение рО2 , уменьшение концентрации гидрокарбоната.
Угнетает дыхательный центр снижение рС02 и увеличение рО2 , увеличение концентрации гидрокарбоната.
Снижение уровня НСО3– в плазме крови (метаболический ацидоз), возникающее первично, компенсируется увеличением легочной вентиляции и снижением рС02, при этом соотношение рС02 /НСО3– остается неизменным.
При тяжелом метаболическом ацидозе стимуляция вентиляции легких доходит до крайнего предела (рС02 ниже 20 мм рт.ст. и даже ниже 10 мм рт.ст.), и дальнейшая компенсация становится невозможной.
Увеличение содержания НСО3– в плазме крови (метаболический алкалоз), возникающее первично, компенсируется снижением легочной вентиляции и увеличением рС02. Как правило, выраженный дыхательный ацидоз не развивается. Тем не менее, при выраженном метаболическом алкалозе существует опасность гиповентиляции и гиперкапнии.
Компенсаторные реакции начинаются сразу же при изменении содержания НСО3–. Максимум компенсации достигается через 12- 24 часа.
Компенсаторные реакции замедленного типа
Основной компенсаторный механизм при дыхательных нарушениях. Суть данного механизма сводится к выведению в большей или меньшей степени Н+ нелетучих кислот и также реабсорбции NаHC03 — обеспечивается функцией почек (аммониогенез, титрование Н+, реабсорбция).
Первичное снижение рС02 (дыхательный алкалоз) способствует подавлению реабсорбции бикарбоната в канальцах почек и задержке ионов Н+, в результате чего снижается содержание НСО3– в плазме крови и компенсаторно развивается метаболический ацидоз.
Первичная гиперкапния (дыхательный ацидоз) сопровождается увеличением реабсорбции бикарбоната и усилением выведения ионов Н+, компенсаторно развивается метаболический алкалоз.
Эти компенсаторные реакции в отличие от реакций немедленного типа происходят длительное время – 6 -12 часов и достигают максимума через несколько суток. Быстрое возрастание рС02 – острый дыхательный ацидоз не компенсируется почками и может привести к летальному исходу без заметного содержания бикарбоната в крови. В отличие от острого, медленно прогрессирующий дыхательный ацидоз (хронический) компенсируется увеличением уровня бикарбоната в крови и прямой угрозы для жизни не представляет.
Определение первичного нарушения КЩС
Снижение или повышение одного показателя — рН крови – свидетельствует об ацидозе или алкалозе, но не дает исчерпывающего ответа на вопрос, какой компонент КЩС нарушен: респираторный или метаболический.
Если же интерпретируются два показателя (рН и рС02), то определение первичности нарушения КЩС становится возможным (таб. 1).
Таблица 1. Определение первичности нарушения КЩС
|
рН артериальной крови (норма 7,35 – 7,45) |
рС02 (норма 35 -45 мм рт.ст.) | Первичное нарушение |
| Снижен | Повышено | Дыхательный ацидоз |
| Снижен | Норма или снижено | Метаболический ацидоз |
| Повышен | Повышено или норма | Метаболический алкалоз |
| Повышено | Снижено | Дыхательный алкалоз |
| Норма | Понижено |
Смешанная форма дыхательного алкалоза и метаболического ацидоза |
| Норма | Повышено |
Смешанная форма дыхательного ацидоза и метаболического алкалоза |
Кислотно-основной гомеостаз крови характеризуют следующие показатели:
рН — показатель активной реакции крови; суммарно отражает функциональное состояние дыхательных и метаболических компонентов и изменяется в случае превышения возможностей всех буферных систем (в норме 7,35 — 7,45).
рСО2 (мм рт. ст.) — напряжение углекислоты в крови; единственный дыхательный показатель КОГ, отражающий функциональное состояние системы дыхания, изменяющееся при ее патологии и в результате компенсаторных реакций при метаболических сдвигах (в норме 35-45 мм рт.ст. в артериальной крови).
АВ (ммоль/л) — истинные бикарбонаты крови (aktual bikarbonate); концентрация ионов угольной кислоты, НС03— при физическом состоянии крови в кровеносном русле, т. е. определенное без соприкосновения с воздухом при температуре 38°С (в норме 21,8-27,2 ммоль/л).
SВ (ммоль/л) — стандартный бикарбонат (standart bikar-bonate); концентрация бикарбонатных ионов (НС03—, измеренная при стандартных условиях: рС02 — 5,3 кПа (40 мм рт. ст.), при температуре 38°С и полном насыщении гемоглобина кислородом. Характеризует смещение ионов бикарбонатной системы.
Этот показатель считается более ценным в диагностическом отношении, чем истинный бикарбонат, поскольку отражает только метаболические сдвиги (в норме 21,6—26,9 ммоль/л).
ВВ (ммоль/л) — буферные основания крови (buffer base); общая концентрация буферных ионов бикарбонаты, белки, гемоглобин в полностью оксигенированной крови. Диагностическое значение этого показателя небольшое, т.к. он меняется в зависимости от рС02, концентрация гемоглобина (в норме 43,7-53,5 ммоль/л).
BE (ммоль/л) — избыток или недостаток буферных оснований (base excess). Характеризует сдвиг ионов всех буферных систем и указывает на природу нарушений кислотно-основного гомеостаза. Отрицательное значение BE отражает дефицит оснований или избыток кислот. При метаболических сдвигах КОГ крови смещение BE будет выражено более значительно, чем при дыхательных нарушениях (в норме BE = -3 — + 3 ммоль/л).
АР- анионная разница. В основе клинического применения показателя АР лежит предположение, что любой раствор, включая плазму, должен быть электронейтральным, т.е. сумма катионов равна сумме анионов. Плазма содержит один главный измеряемый катион Na+ и два главных измеряемых аниона СI— и НСОз—. Вклад других неизмеряемых анионов (НА) и катионов (НК) невелик (таб. 2). Из этого следует, что сумма измеряемых и неизмеряемых анионов равна сумме измеряемых и неизмеряемых катионов:
НА + (СI— + НСОз—) = НК + Na+
Таблица 2. Анионная разница
Пользуясь данными таблицы можно рассчитать АР:
АР = НА – НК = 23 – 11 = 12 мэкв/л
АР = НА – НК = Na+- (СI— + НСОз—)
В случаях увеличения Н+ неравенство между измеряемыми в плазме концентрациями катионов и анионов выйдет за пределы нормального диапазона 9 – 13 мэкв/л.
Показатель АР может быть полезен для выявления этиологии метаболического ацидоза.
Как правило, чем больше АР, тем легче определить причину ацидоза.
Высокая АР характерна для лактат-ацидоза, вызванного анаэробным гликолизом. Диабетический кетоацидоз и уремия также сопровождается увеличением АР. Если при высокой АР уровень лактата, кетона и креатинина нормальный, наиболее вероятно, что причиной ацидоза является прием токсичных веществ (метанол, паральдегид, этанол, этиленгликоль, лекарственные средства). Высокий уровень салицилатов в плазме сопровождается значительным увеличением АР.
Классификация нарушений КЩС
1. Простые нарушения:
Ацидоз:
— метаболический
— респираторный
Алкалоз:
— метаболический
— респираторный
2.1 Однонаправленные: метаболический и дыхательный ацидоз и алкалоз
2.2 Разнонаправленные:
— метаболический ацидоз и дыхательный алкалоз
— метаболический алкалоз и дыхательный ацидоз
Значения рН остаются в пределах нормы (рН=7,35 — 7,45), содержание бикарбонатов и СО2 изменяется в зависимости от направленности метаболических и респираторных сдвигов.
Кроме изменений в содержании бикарбонатов и СО2 изменяется и рН, но в незначительных пределах + 0,04 (рН=7,31 – 7,49)
рН < 7,30 – некомпенсированный ацидоз;
рН > 7,50 – некомпенсированный алкалоз.
Метаболический ацидоз
Метаболический ацидоз возникает вследствие существенного снижения уровня бикарбоната в организме.
1. Увеличение продукции нелетучих кислот.
Усиленная продукция кислых метаболитов (так называемых кетокислот — (3-гидроксибутирата и ацетоацетата) является одной из характерных особенностей неконтролируемого или плохо контролируемого инсулинзависимого диабета. При этом состоянии, называемом диабетическим кетоацидозом, количество бикарбоната в крови значительно снижается из-за его использования для нейтрализации избытка кислот.
В клетках, которые в значительной мере лишены кислорода и, поэтому, не могут метаболизировать (окислять) глюкозу происходит накопление лактата. Такое существенное накопление лактата в крови в количествах, достаточных для развития метаболического ацидоза, происходит, если ткани неадекватно перфузируются кровью, а следовательно и недостаточно оксигенируются.
Наиболее яркой причиной лактоацидоза при нарушении перфузии тканей является гиповолемический шок. Кроме того, лактоацидоз может возникать при почечной или печеночной недостаточности, диабете, сепсисе и лейкемии.
2. Увеличение потерь оснований.
Бикарбонат секретируется в полость тонкого кишечника для осуществления пищеварения и абсорбируется в нижних отделах желудочно-кишечного тракта. Если реабсорбции не происходит, он теряется с фекалиями.
Любые заболевания пищеварительного тракта (например, тяжелая диарея) могут привести к потерям бикарбоната из организма в количествах, достаточных для развития метаболического ацидоза.
Также потеря бикарбонатов может быть связана с почечной недостаточностью (проксимальный канальцевый ацидоз – почечный ацидоз II типа). Ухудшение реабсорбции Nа+ приводит появлению щелочной реакции мочи. Кроме этого, проксимальный канальцевый ацидоз характеризуется снижением уратов, фосфатов и калия в сыворотке крови, глюкозурией и аминоацидурией.
С помощью величины АР можно отличить потери НСОз— при диарее от потерь НСОз—, вызванных почечным канальцевым ацидозом таб. 3.
Таблица 3. Анионная разница по (П.Марино, 1998)
|
АР мочи АР = (Nа+ + К+) – СI- |
рН мочи | диагноз |
|
Отрицательная Положительная Отрицательная |
<5,5
>5,5 >5,5 |
Патологии нет Почечный канальц. ацидоз Диарея |
3. Увеличение поступлений в организм кислот извне.
Злоупотребление кислой пищей, прием внутрь соляной кислоты, введение в больших количествах старой консервированной крови
4. Уменьшение выведения ионов Н+ через почки.
В нормальных условиях почки выводят Н+ в виде титруемой кислоты (фосфаты, сульфаты) и аммиака. Этот механизм может быть нарушен при заболеваниях почек, недостаточности надпочечников, дистальном почечном канальцевом ацидозе и гиперальдостеронизме. При почечной недостаточности, уменьшении числа функционирующих нефронов адекватная фильтрация и выведение Н+ отсутствуют.
При почечном ацидозе I типа (дистальный канальцевый ацидоз) секреция Н+ в дистальных канальцах нарушается. Поскольку экскреция Н+ в дистальных канальцах зависит от обмена Nа+ , уменьшение объема жидкости способствует нарастанию ацидоза. Посредством такого же механизма, связанного с уменьшением поставки Nа+ в канальцы почек, адреналиновая недостаточность и селективный гипоальдостеронизм также приводят к ухудшению экскреции Н+. При этом метаболический ацидоз сочетается с другими формами нарушений электролитного обмена: гиперкалиемией, гипонатриемией, гиперкальциемией.
Снижение уровня НСО3– в плазме крови (метаболический ацидоз), возникающее первично, компенсируется увеличением легочной вентиляции и снижением рС02, при этом соотношение рС02 /НСО3– остается неизменным.
Увеличение содержания кислот буферируется бикарбонатным буфером:
НС1 + H 2C03/NаHC03 ↔ Nа Сl+ H 2C03
↓
С02 + Н2О
Диагностические критерии:
1. При сниженном рН нормальный или пониженный уровень рСО2 указывает на первичный метаболический ацидоз;
2. При нормальной величине рН пониженный уровень рСО2 указывает на смешанную форму дыхательного алкалоза и метаболического ацидоза;
3. При нормальной величине рН нормальный уровень рСО2 может свидетельствовать о том, что показатели КЩС находятся в пределах нормы, но не исключается возможность смешанных метаболических алкалозов/ацидозов.
В этих случаях определяют АР и по этому показателю судят об изменениях КЩС.
4. Дефицит оснований – АВ, ВЕ, ВВ, SВ.
Клинические формы ацидоза
Лактат – ацидоз
Этиопатогенез.
1. Снижение оксигенации тканей – тканевая гипоксия. Наибольшее значение придают циркуляторным нарушениям (кардиогенный, септический, гиповолемический шок). Наличие всех форм гипоксии теоретически способствует развитию лактат-ацидоза. Остановка сердца сопровождается анаэробным обменом веществ и лактат-ацидозом;
2. Нарушения функции печени снижают ее способность к превращению молочной кислоты в глюкозу и гликоген.
3. Недостаток тиамина (витамин В1) у больных, злоупотребляющих алкоголем ведет к угнетению окисления пирувата в митохондриях и способствует накоплению молочной кислоты.
4. Повышение правовращающего изомера молочной кислоты (D-лактат-ацидоз), неопределяемого стандартными лабораторными методиками. Это изомер образуется в результате действия микроорганизмов, расщепляющих глюкозу в кишечнике. Чаще всего встречается у больных после обширных операций на кишечнике, при дисбактериозе, нарушениях функции ЖКТ. По-видимому, это наиболее распространенное нарушение КЩС, но оно часто не диагностируется (П.Марино, 1998);
5. Не исключается возможность лактат-ацидоза при длительных инфузиях адреналина и других сосудосуживающих средств.
6. Лактат-ацидоз может развиться в случаях использования натрия нитропруссида, при метаболизме которого образуются цианиды, способные нарушать процессы окислительного фосфорилирования.
Диагностика лактат-ацидоза:
— наличие метаболического ацидоза, связанного с повышенной АР;
— выраженный дефицит оснований;
— АР>30 мэкв/л, в то время как другие причины, вызывающие ацидоз (кетоацидоз, почечная недостаточность, введение токсических веществ), отсутствуют;
— уровень молочной кислоты в венозной крови превышает 2 мэкв/л. Этот показатель отражает интенсивность образования лактата в тканях.
Устранение причины лактат-ацидоза.
Введение натрия бикарбоната показано при рН<7,2, содержании НСОз— <15 ммоль/л. Расчет примерной дозы натрия бикарбоната можно провести по следующей формуле:
Дефицит НСОз—(ммоль) = 0,3 * масса тела (кг) * ВЕ = мл 8,5%р-р соды
Для 3% соды: ВЕ*0,8*масса тела
Для 4% соды: ВЕ*0,6*масса тела
Для 5% соды: ВЕ*0,5*масса тела
Вначале устраняют половину выявленного дефицита НСОз путем внутривенного введения раствора в течение 30 минут. Затем под контролем содержания НСОз в сыворотке крови продолжают коррекцию в течение 4 – 6 часов.
Пример:
В данном случае рН ниже нормы — обозначается как некомпенсированный ацидоз. Далее оцениваем газовый состав крови: уровень рО2 для артериальной крови несколько повышен, но рСО2 снижен. Учитывая дефицит оснований и повышенный лактат можно сделать вывод, что это метаболический лактат-ацидоз, при котором включена немедленная компенсация в виде гипервентиляции.
Кетоацидоз.
В условиях выраженного дефицита инсулина блокируется поступление глюкозы в мышцы и жировую ткань, снижается уровень глюкозы в клетках, ткани испытывают «энергетический голод». Это ведет к гиперсекреции контринсулярных гормонов – соматотропина, глюкагона, кортизола, адреналина. Под влиянием этих гормонов стимулируется гликогенолиз, глюконеогенез и липолиз. В результате липолиза жиры расщепляются до свободных жирных кислот, которые становятся источником энергии и кетоновых тел. В условиях дефицита инсулина происходит чрезмерное образование кетоновых тел, развивается кетоацидоз.
— слабость, жажда, тошнота;
— диабетическая прекома;
— диабетическая кома.
— гипергликемия
— глюкозурия
— метаболический ацидоз (снижение рН, НСОз, рСО2, выраженный дефицит оснований)
— ацетон в плазме
— ацетонурия
— гиперосмолярность плазмы > 300 мосм/л
Первоначальная доза инсулина 10 ЕД в/в. Последующую инфузию инсулина в изотоническом растворе натрия хлорида или 5% раствре глюкозы проводят со скоростью 0,1 ЕД/кг/час.
Дефицит внеклеточной и внутриклеточной жидкости при кетоацидозе может достигать 10% массы тела. Лечение следует начинать с введения изотонических растворов, содержащих Na+ и CI—. Опасность чрезмерного введения кристаллоидов заключается не только в перегрузке объёмом, но и в дисбалансе концентраций натрия и глюкозы. Поэтому необходим динамический контроль этих веществ и при необходимости своевременная коррекция.
Потери К+ при кетоацидозе достигают 200 – 700 ммоль и продолжаются по мере устранения ацидоза. Проводя коррекцию гипокалиемии необходимо учитывать не только дефицит, но и потребность. Представлена формула расчета дефицита К+:
Дефицит калия (ммоль) = масса больного (кг) х 0,2 х (4,5 – К+ плазмы)
Рекомендуется введение натрия бикарбоната при снижении рН < 7,2 и снижении АДсист ниже 90 мм рт.ст., для предупреждения дальнейших электролитных нарушений и гемолиза. Но введение раствора соды должно быть более осторожным, чем при лактат-ацидозе, рекомендуется вводить 1/2 расчетной дозы.
— превращение этанола в процессе метаболизма в печени в ацетальдегид с образованием НАД-Н, способствующего выработке кетоновых тел;
— сопутствующее голодание, сопровождающееся усилением кетогенеза и кетонемией;
— обезвоживание, ведущее к олигурии и снижению экскреции кетоновых тел с мочой.
Алкогольный кетоацидоз обычно развивается через 1 – 3 дня после чрезмерного потребления спиртных напитков. Как правило, уровень глюкозы и кетоновых тел повышается не очень высоко.
Показано в/в введение изотонического раствора натрия хлорида и 5% глюкозы.
Глюкоза угнетает образование кетоновых тел в печени, а солевые растворы повышают выведение их с мочой. Коррекцию калия проводят по содержанию его в сыворотке крови. натрия бикарбонат применим только если рН < 7,2 и снижении АДсист ниже 90 мм рт.ст..
Пример:
Интерпретация анализа начинается с рН. В данном случае рН ниже нормы и обозначается как некомпенсированный ацидоз. Далее оцениваем газовый состав крови: уровень рО2 для венозной крови нормальный, однако сделать заключение о наличие гипоксемии нельзя, для этого необходимо определить рО2 в артериальной крови. Но с учетом нормального уровня лактата, можно сделать вывод, что дефицита О2 нет, идет аэробный гликолиз. Генез ацидоза метаболический и данное заключение можно сделать по уровню дефицита оснований.
Снижение уровня бикарбоната может быть связано с метаболическим ацидозом или развившейся почечной недостаточностью, это можно сказать с учетом анамнестических и клинических данных.
— Потеря нелетучих кислот
Тяжелая и длительная рвота желудочным соком (он кислый) приводит к потере НСI из организма. Это причины метаболического алкалоза, ассоциированного со стенозом привратника — состояния, при котором затрудняется продвижение желудочного содержимого в тонкий кишечник.
— Потеря ионов Н+
Гипокалиемия увеличивает проксимальную канальцевую реабсорбцию НСОз и повышает дистальную канальцевую секрецию Н+. Повышение уровня албдостерона увеличивает секрецию Н+.
— Избыточное введение бикарбоната натрия.
В данном случае алкалоз развивается при неконтролируемом введении бикарбоната, цитрата, лактата или ацетата.
Компенсаторные механизмы:
Увеличение содержания НСО3– в плазме крови (метаболический алкалоз), возникающее первично, компенсируется снижением легочной вентиляции и увеличением рС02. Как правило, выраженный дыхательный ацидоз не развивается. Тем не менее, при выраженном метаболическом алкалозе существует опасность гиповентиляции и гиперкапнии.
NаОН + H 2C03/NаHC03 ↔ 2NаHC03 + Н2О
— НСОз в артериальной крови более 25 ммоль/л, в венозной крови – более 30 ммоль/л;
— рН выше нормального уровня;
— рСО2 нормальное или повышенное, в наиболее тяжелых случаях может быть сниженным;
— при гипохлоремическом алкалозе – СI менее 100 ммоль/л;
— часто бывает гипокалиемия.
1.Устранение основной причины алкалоза;
2.Восполнение дефицита: Дефицит СI (моль/л) = 0,27* масса тела (кг) * (100 – фактическое содержание СI)
Необходимый объём изотонического раствора натрия хлорида может быть определен по формуле: NаСI (л) = дефицит СI / 154, где 154 – содержание СI (моль/л) в 1 л 0,9% раствора натрия хлорида;
3.При потерях НСI необходимо в/в раствора НСI. Обязательное условие для его назначения – нормальное содержание жидкости в организме и нормальная концентрация К+ в сыворотке крови. Дефицит водорода определяют по следующей формуле:
Дефицит Н+ = 0,5 * масса тела (кг) *
(фактическое содержание HC03 – желаемое содержание HC03)
В 1 л 0,1 нормального раствора HC03 содержится 100 ммоль Н+. скорость введения раствора НСI – 0,2 ммоль/кг/час.
Максимальная суточная доза раствора НСI = 100 ммоль.
При неосложненном метаболическом алкалозе содержание HC03 в сыворотке крови менее 35 ммоль/л считают относительно безопасным.
4.Устранение гипокалиемии (см. выше).
Пример:
В данном случае рН выше нормы и обозначается как некомпенсированный алкалоз. Далее оцениваем газовый состав крови: уровень рСО2 несколько повышен, а рО2 в пределах нормы, следовательно алкалоз не респираторного происхождения. Генез алкалоза однозначно метаболический, что подтверждает избыток оснований.
Дыхательный ацидоз.
— Острая дыхательная недостаточность;
— Хроническая дыхательная недостаточность.
Острый дыхательный ацидоз.
Острый дыхательный ацидоз представляет угрозу для жизни больного, характеризуется первичным острым накоплением СО2 в жидких средах организма из-за снижения альвеолярной вентиляции, ограничивающей элиминацию СО2. Однако наряду с увеличением содержания в крови СО2, как правило наблюдается снижение рО2 в артериальной крови.
Первичная гиперкапния (дыхательный ацидоз) сопровождается увеличением реабсорбции бикарбоната и усилением выведения ионов Н+ почками, компенсаторно развивается метаболический алкалоз. Но эта компенсаторная реакция относится к реакции замедленного типа, которая происходит длительное время (6-12 часов) Клетки почечных канальцев богаты ферментом карбоангидразой, которая катализирует синтез угольной кислоты из углекислого газа и воды. Угольная кислота диссоциирует с освобождением бикарбоната, который выходит в кровь (для восполнения бикарбонатного буфера), и ионов водорода, которые эксретируются с мочой.
В крови действие фосфатного буфера сводится к поддержанию и воспроизводству бикарбонатного буфера. При увеличении в крови кислот и образовании Н2С03 происходит обменная реакция:
H++HC03— + Na2HP04 = NaHC03 + NaH2P04
Избыток Н2С03 ликвидируется, а концентрация НС03— увеличивается.
Остро возникшее увеличение содержания СО2 в крови в первую очередь проявляется изменениями функции ЦНС и в меньшей степени сердечно-сосудистой системы. Потеря сознания является результатом интраневрельного ацидоза, усиления мозгового кровотока и увеличения ВЧД, за счет гиперкапнии и дилатации сосудов мозга. Системное сосудорасширяющее действие гиперкапнии проявляется гиперемией кожных покровов, повышенной потливостью, тахикардией.
Восстановление адекватной вентиляции легких и оксигенации крови, под контролем рСО2 и рО2 в артериальной крови. Одновременно проводят лечение основного заболевания, вызвавшего острый дыхательный ацидоз.
Хронический дыхательный ацидоз.
Хронические обструктивные заболевания легких.
Хронический дыхательный ацидоз развивается длительное время, компенсация может быть полной, и тогда рН не выходит за пределы нормы при повышенном рСО2 в артериальной крови и соответствующем возрастании НСО3. При отсутствии достаточных механизмов компенсации хронический дыхательный ацидоз может быть субкомпенсированным. Обычно повышение рСО2 сопровождается умеренным снижением рН и увеличением уровня НСО3. Из организма при этом выводятся Н+,CI— и NН4CI, обладающий свойствами сильной кислоты. Компенсаторный характер метаболического алкалоза очевиден. Несмотря на почечную компенсацию, дыхательные нарушения могут прогрессировать.
Хронический дыхательный ацидоз может перейти в острый, и тогда он представляет угрозу для жизни больного.
Профилактика и лечение основного заболевания.
Пример:
В данном случае рН ниже нормы — обозначается как некомпенсированный ацидоз. Оцениваем газовый состав крови: уровень рО2 для венозной крови нормальный, однако сделать заключение о наличие гипоксемии нельзя, для этого необходимо определить рО2 в артериальной крови. Но с учетом нормального уровня лактата, можно сделать вывод, что дефицита О2 нет, идет аэробный гликолиз. Но повышенный уровень рСО2 говорит о дыхательном ацидозе. Тактика коррекции будет зависеть от клиники.
Дыхательный алкалоз.
— нарушения функции ЦНС;
— болевой синдром;
— возбуждение;
— ИВЛ в режиме гиповентиляции.
Первичное снижение рС02 (дыхательный алкалоз) способствует подавлению реабсорбции бикарбоната в канальцах почек и задержке ионов Н+, в результате чего снижается содержание НСО3– в плазме крови и компенсаторно развивается метаболический ацидоз.
Патофизиологические изменения.
Доказано, что острая гипокапния сопровождается снижением содержания бикарбонатов и концентрации Н+ не только в артериальной крови, но и в цереброспинальной жидкости. Острая гипокапния снижает мозговой кровоток, что приводит к гипоксии мозга и увеличению образования в мозге лактата.
При острой гипокапнии возможны значительное снижение сердечного выброса, повышение ОПСС, что ведет к значительному уменьшению перфузии тканей и увеличению содержания лактата в плазме.
Обычными признаками острого алкалоза являются тахипноэ и одышка. При хроническом алкалозе частота дыхания может оставаться нормальной при повышенном дыхательном объёме. Признаки дыхательного алкалоза не специфичны и проявляются нарушением нейромышечной функции (парестезии, судороги, тремор).
Специального лечения не требуется, важно выявить и устранить основную причину, вызвавшую это нарушение.
Пример:
В данном случае рН выше нормы и обозначается как некомпенсированный алкалоз.
Учитывая, что рСО2 ниже нормы, уровень лактата в норме и нет избытка оснований, можно говорить о чистом дыхательном алкалозе. Тактика коррекции будет зависеть от клиники.
При гипокапнии и одновременном повышении уровня лактата с метаболическим ацидозом, необходимо думать о циркуляторной или тканевой гипоксии – низкой продукции углекислоты тканями при анаэробном гликолизе.
Это чрезвычайно опасная ситуация, сопровождающаяся нормальной сатурацией и нормальным напряжением кислорода, что успокаивает врача. Подтверждением этому опасному состоянию служит низкая артерио-венозная разница по кислороду.
Литература
1. Бунятян А.А., Рябов Г.А., Маневич А.3. Анестезиология и реаниматология. 2-е изд. перераб. и доп. М., Медицина 1984
2. Дэвид М.Габа, Кевин Дж.Фиш, Стивен К.Хауард. Критические ситуации в анестезиологии. Перевод с англ. –М.М. -2000 г.
3. Малышев В.Д. Интенсивная терапия острых водно-электролитных нарушений. М.:Медицина,1985. 192 с.
4. Малышев В.Д. Интенсивная терапия. Реанимация. Первая помощь: Учебное пособие. — М.: Медицина.— 2000.— 464 с
5. Уилкинсон А.У. Водно-электоролитный обмен в хирургии / Пер. с англ. М.: Медицина 1974
6. Шмидт Р., Тевс Г. /ред./ Физиология человека. /пер. с англ./ М., 1986, т.3.
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.

Биохимические маркеры утомления и восстановления после физической нагрузки

В настоящее время появляется потребность оценки степени физической нагрузки или уровня жизнеспособности организма и его элементов, что является одной из ключевых задач профилактики травм и оценки степени тренированности футболистов. Такая оценка позволяет объективно зарегистрировать темп изнашиваемости организма и его изменения при лечебно-профилактических воздействиях. Существуют различные подходы к получению данной оценки, например можно измерять степень отклонения различных структурно-функциональных характеристик организма от нормы и таким образом оценивать степень их утомления и восстановления или износа. Однако, для разных органов и систем организма типичным является разновременное начало, разная степень выраженности и разнонаправленность этих изменений (обычно как результат развития компенсаторных процессов). Зачастую выявляется выраженное индивидуальное и видовое различие этих изменений. При выборе показателей для оценки интенсивности физической нагрузки (ФН) и утомляемости из огромного множества возможных биомаркеров следует учитывать ряд требований, выполнение которых существенно повышает информативность и качество оценки:
1. Показатель обязательно должен значительно изменяться (желательно в несколько раз) в промежутке времени от начала тренировки до периода восстановления (отдыха).
2. Показатель должен быть высоко коррелированным со степенью ФН и тренированностью спортсмена.
3. Межиндивидуальная дисперсия показателя не должна превышать величины изменения его среднего значения.
4. Должна иметь место низкая чувствительность выбранного показателя к болезням (болезни не должны имитировать изменение показателя).
5. Обязательно должно наблюдаться изменение показателя для всех членов популяции.
6. Показатель должен быть индикатором достаточно значимого процесса возрастной физиологии и должен иметь смысловую, морфологическую и функциональную интерпретацию, отражать степень физической тренированности организма или изношенности какой — либо системы.
Кроме этого, при определении биохимического маркера ФН желательно:
· учитывать показатели возраста;
· предусмотреть оценку степени тренированности по системам и органам;
· учитывать апробированные в мировой практике тесты и формулы;
· использовать современные средства информатики.
К настоящему времени, к сожалению, не имеется сравнительного анализа наборов биохимических показателей по каким-либо критериям качества. Пока что не удается однозначно ответить на вопрос, какое же число показателей оптимально для определения степени ФН и утомляемости. Ясно, однако, что увеличение числа показателей более 10-15 мало что дает в отношении точности определения ФН. Небольшое число показателей (3-4) не позволяет дифференцировать типы и профиль ответа организма на ФН.
В различных странах было сделано немало попыток использовать изменение биохимических параметров в качестве маркеров физиологической утомляемости, но все они были неизменно сопряжены с рядом трудностей, связанных с отсутствия четких нормативов. Поскольку различные системы и органы неравномерно реагируют на ФН, основное значение приобретает выбор наиболее информативного, «ведущего» для данного вида тренировки критерия. Очень важна его скоррелированность с другими параметрами биохимического статуса и одинаковость (тождество) состояния признака по завершению процессов утомляемости.
До конца нерешенным остается вопрос о том, какие же показатели максимально пригодны для определения утомляемости у футболистов ввиду их значительной физиологической и индивидуальной вариации. Для ответа на этот вопрос полезно учитывать отношение изменения показателя в течение тренировочного процесса к межиндивидуальному разбросу.
Приказ 337 2001 года (выписка)
3.2. Лабораторные исследования:
3.2.1. Клинический анализ крови;
3.2.2. Клинический анализ мочи;
3.2.3. Клинико — биохимический анализ крови из вены для:
— Определения регуляторов энергетического метаболизма: кортизола, тестостерона, инсулина;
-Оценки тиреоидного статуса: Т3 общий, Т4 общий, ТТГ(тиреотропин);
— Оценки уровня ферментов: АЛТ (аланинаминотрансфераза), ACT (аспартатаминотрансфераза), Щелочная фосфотаза, КФК (креатинфосфокиназа).
— Оценки биохимических показателей: глюкозы, холестерина, триглицеридов, фосфора.
Все перечисленные показатели практически в произвольных сочетаниях используются теми ли иными школами по определению степени утомляемости. Оптимальным, видимо, является набор из наиболее отличающихся тестов, охватывающих различные системы и органы и отражающий:
· возрастную физиологию,
· пределы адаптации и функциональные резервы,
· физическую и нервно-психическую работоспособность,
· характеристики наиболее важных систем.
В практике спорта обычно используется определение активности и содержания;
• энергетических субстратов (АТФ, КрФ, глюкоза, свободные жирные кислоты);
• ферментов энергетического обмена (АТФ-аза, КрФ-киназа, цитохромоксидаза, лактатдегидрогеназа и др.);
• промежуточных и конечных продуктов обмена углеводов, липидов и белков (молочная и пировиноградная кислоты, кетоновые тела, мочевина, креатинин, креатин, мочевая кислота, углекислый газ и др.);
• показателей кислотно-основного состояния крови (рН крови, парциальное давление СО2, резервная щелочность или избыток буферных оснований и др.);
• регуляторов обмена веществ (ферменты, гормоны, витамины, активаторы, ингибиторы);
• минеральных веществ в биохимических жидкостях (бикарбонаты и соли фосфорной кислоты определяют для характеристики буферной емкости крови);
• белка и его фракций в плазме крови.
В настоящем докладе мы ограничимся общим обзором предлагаемых показателей, систематизацией их по классам и возможностью использованием для оценки интенсивности воздействия ФН на различные системы организма. Как показывают исследования, по изменениям субстратов, происходящих в тренированном организме и находящих своё отражение, как в структуре мышц, так и в интегральной форме — в крови, являются отражением окислительных процессов в мышцах. Изучая скорость мобилизации и утилизации энергетических субстратов, при том или ином виде нагрузки в динамике тренировочного процесса, можно составить представления о том, в какой фазе находится формирование основного качества, определяющего выносливость, скоростно-силовые качества, окислительные способности работающих мышц.
Показатели углеводного обмена.
Глюкоза. Изменение ее содержания в крови при мышечной деятельности индивидуально и зависит от уровня тренированности организма, мощности и продолжительности физических упражнений. Кратковременные физические нагрузки субмаксимальной интенсивности могут вызывать повышение содержания глюкозы в крови за счет усиленной мобилизации гликогена печени. Длительные физические нагрузки приводят к снижению содержания глюкозы в крови. У нетренированных лиц это снижение более выражено, чем у тренированных. Повышенное содержание глюкозы в крови свидетельствует об интенсивном распаде гликогена печени либо относительно малом использовании глюкозы тканями, а пониженное ее содержание — об исчерпании запасов гликогена печени либо интенсивном использовании глюкозы тканями организма.
По изменению содержания глюкозы в крови судят о скорости аэробного окисления ее в тканях организма при мышечной деятельности и интенсивности мобилизации гликогена печени. Этот показатель обмена углеводов редко используется самостоятельно в спортивной диагностике, так как уровень глюкозы в крови зависит не только от воздействия физических нагрузок на организм, но и от эмоционального состояния человека, гуморальных механизмов регуляции, питания и других факторов.
Появление глюкозы в моче при физических нагрузках свидетельствует об интенсивной мобилизации гликогена печени. Постоянное наличие глюкозы в моче является диагностическим тестом заболевания сахарным диабетом.
Органические кислоты. Этот анализ позволяет обнаруживать метаболические нарушения, связываемые с генерализованной болью и утомляемостью, причинами возникновения которых считают реакцию на токсическую нагрузку, дисбаланс питательных веществ, пищеварительную дисфункцию и другие факторы. Этот анализ позволяет получить важную клиническую информацию о: органических кислотах, которые точно отражают углеводный метаболизм, функцию митохондрий и бета-окисление жирных кислот; дисфункции митохондрий, которая может лежать в основе хронических симптомов фибромиалгии, утомляемости, недомоганий, гипотонии (ослабления мышечного тонуса), нарушения кислотно-основного баланса, низкой переносимости физических нагрузок, боли в мышцах и суставах, а также головной боли. Нормальное здоровье и самочувствие зависят от здорового функционирования клеток. В каждой клетке имеется митохондрия, работающая как «электростанция». Основная функция митохондрии — эффективно производить требуемую для жизни энергию. Профиль клеточной энергии измеряет специально подобранные группы органических кислот. Эти метаболиты в основном отражают углеводный метаболизм, функционирование митохондрий и окисление жирных кислот, которое происходит в процессе дыхания клетки. Измеряемые в ходе данного анализа органические кислоты являются основными компонентами и промежуточными элементами метаболических путей преобразования энергии, связанных с циклом Кребса и производством аденозинтрифосфата — основного источника энергии клеток. Этот профиль может оказаться особенно полезным для пациентов с хроническим недомоганием, фибромиалгией, утомляемостью, гипотонией (ослаблением мышечного тонуса), нарушением кислотно-щелочного баланса, плохой переносимостью физических нагрузок, болями в мышцах или суставах, а также головной болью. Органические кислоты играют главенствующую роль в выработке энергии для мышечной ткани. Поэтому дефекты митохондрий связаны с множеством нервно-мышечных нарушений. Накопление лактата, естественного для анаэробного гликолиза вещества, в плазме свидетельствует об истощении окислительного метаболического потенциала вследствие возрастания энергетических потребностей. Гликолитический механизм ресинтеза АТФ в скелетных мышцах заканчивается образованием молочной кислоты, которая затем поступает в кровь. Выход ее в кровь после прекращения физической нагрузки происходит постепенно, достигая максимума на 3—7-й минуте после окончания ФН. Содержание молочной кислоты в крови существенно возрастает при выполнении интенсивной физической работы. При этом накопление ее в крови совпадает с усиленным образованием в мышцах. Значительные концентрации молочной кислоты в крови после выполнения максимальной работы свидетельствуют о более высоком уровне тренированности при хорошем спортивном результате или о большей метаболической емкости гликолиза, большей устойчивости его ферментов к смещению рН в кислую сторону. Таким образом, изменение концентрации молочной кислоты в крови после выполнения определенной физической нагрузки связано с состоянием тренированности спортсмена. По изменению ее содержания в крови определяют анаэробные гликолитические возможности организма, что важно при отборе спортсменов, развитии их двигательных качеств, контроле тренировочных нагрузок и хода процессов восстановления организма.
Показатели липидного обмена.
Свободные жирные кислоты. Являясь структурными компонентами липидов, уровень свободных жирных кислот в крови отражает скорость липолиза триглицеридов в печени и жировых депо. В норме содержание их в крови составляет 0,1—0,4 ммоль • л»1 и увеличивается при длительных физических нагрузках.
По изменению содержания СЖК в крови контролируют степень подключения липидов к процессам энергообеспечения мышечной деятельности, а также экономичность энергетических систем или степень сопряжения между липидным и углеводным обменом. Высокая степень сопряжения этих механизмов энергообеспечения при выполнении аэробных нагрузок является показателем высокого уровня функциональной подготовки спортсмена.
Кетоновые тела. Образуются они в печени из ацетил-КоА при усиленном окислении жирных кислот в тканях организма. Кетоновые тела из печени поступают в кровь и доставляются к тканям, в которых большая часть используется как энергетический субстрат, а меньшая выводится из организма. Уровень кетоновых тел в крови отражает скорость окисления жиров. При накоплении в крови (кетонемия) они могут появиться в моче, тогда как в норме в моче кетоновые тела не выявляются. Появление их в моче (кетонурия) у здоровых людей наблюдается при голодании, исключении углеводов из рациона питания, а также при выполнении физических нагрузок большой мощности или длительности.
По увеличению содержания кетоновых тел в крови и появлению их в моче определяют переход энергообразования с углеводных источников на липидные при мышечной активности. Более раннее подключение липидных источников указывает на экономичность аэробных механизмов энергообеспечения мышечной деятельности, что взаимосвязано с ростом тренированности организма.
Холестерин. Это представитель стероидных липидов, не участвующий в процессах энергообразования в организме. Однако, систематические физические нагрузки могут привести к его снижению в крови. Можно выделить три типа изменения (повышение, снижение и не изменяющееся) содержание общего холестерина после мышечного усилия. Характер изменений холестерина зависит от его исходного уровня: при более высоком содержании общего холестерина отмечается его снижение в ответ на нагрузку, при относительно низком, наоборот, происходит его увеличение. У спортсменов имеет место увеличение содержания холестерина как в покое, так и после физической нагрузки.
Фосфолипиды. Содержание фосфолипидов отражает выраженность нарушений липидного обмена связанного с дистрофией печени. Повышение их уровня в крови наблюдается при диабете, заболеваниях почек, гипофункции щитовидной железы и других нарушениях обмена, понижение — при жировой дистрофии печени. Поскольку длительные физические нагрузки сопровождаются жировой дистрофией печени, в спортивной практике иногда используют контроль содержания триглицеридов и фосфолипидов в крови.
Продукты перекисного окисления липидов (ПОЛ). При интенсивных физических нагрузках усиливаются процессы перекисного окисления липидов и в крови накапливаются продукты этих процессов, что является одним из факторов, лимитирующих физическую работоспособность. Две составляющие этого механизма: уровень перекисных процессов в скелетной мышце и вовлечение лейкоцитов в процесс повреждения. ФН вызывает усиление перекисных процессов в скелетных мышцах при снижении активности основного фермента антиоксидантной защиты – супероксиддисмутазы, что приводит к повреждению целостности мембран миоцитов. Результатом повреждения клеточной мембраны является изменение ее проницаемости и выход в кровь как цитоплазматических (миоглобин, аспартатаминотрансфераза), так и структурных (тропомиозин) белков скелетной мышцы. Повреждение ткани при гипоксии и вследствие развития процесса перекисного окисления при восстановлении кровотока (реперфузия) стимулирует привлечение в очаг повреждения лейкоцитов которые в следствие активации выделяют большое количество активных форм кислорода (ОМГ-тест) тем самым разрушая здоровые ткани. Через одни сутки после интенсивной физической нагрузки активность гранулоцитов крови выше контрольного значения примерно в 7 раз и на этом уровне сохраняется в течение последующих 3 суток, затем начинает снижаться, превышая, однако, контрольный уровень и через 7 суток восстановления.
Биохимический контроль реакции организма на физическую нагрузку, оценка специальной подготовленности спортсмена, выявления глубины биодеструктивных процессов при развитии стресс-синдрома должены включать определение содержания продуктов перекисного окисления в крови: малонового диальдегида, диеновых конъюгатов, а также активность ферментов глутатионпероксидазы, глутатионредуктазы и каталазы, супероксиддисмутазы. Перекисное повреждение белковых веществ приводит к их деградации и образованию токсических фрагментов, в том числе, молекул средней массы (МСМ), которые принято считать маркерами эндогенной интоксикации в том числе у спортсменов после интенсивной ФН.
Показатели белкового обмена
Гемоглобин. Основным белком эритроцитов крови является гемоглобин, который выполняет кислородтранспортную функцию. Он содержит железо, связывающее кислород воздуха. При мышечной деятельности резко повышается потребность организма в кислороде, что удовлетворяется более полным извлечением его из крови, увеличением скорости кровотока, а также постепенным увеличением количества гемоглобина в крови за счет изменения общей массы крови. С ростом уровня тренированности спортсменов в видах спорта на выносливость концентрация гемоглобина в крови возрастает. Увеличение содержания гемоглобина в крови отражает адаптацию организма к физическим нагрузкам в гипоксических условиях. Однако при интенсивных тренировках, происходит разрушение эритроцитов крови и снижение концентрации гемоглобина, что рассматривается как железодефицитная «спортивная анемия». В таком случае следует изменить программу тренировок, а в рационе питания увеличить содержание белковой пищи, железа и витаминов группы В.
По содержанию гемоглобина в крови можно судить об аэробных возможностях организма, эффективности аэробных тренировочных занятий, состоянии здоровья спортсмена. Гематокрит — это доля (%) от общего объема крови, которую составляют эритроциты. Гематокрит отражает соотношение эритроцитов и плазмы крови и при адаптации к физической нагрузке имеет исключительно важное значение. Определение его позволяет оценить состояние кровообращения в микроциркуляторном русле и определить факторы, затрудняющие доставку кислорода в ткани. Гематокрит при ФН возрастает в результате чего увеличивается способность крови транспортировать кислород к тканям. Однако это имеет и отрицательную сторону — приводит к повышению вязкости крови, что затрудняет кровоток и ускоряет время свертывания крови. Повышение уровня гемоглобина в крови обусловлено уменьшением плазмы крови в результате трансфузии жидкости из кровяного русла в ткани и выходом эритроцитов из депо.
Ферритин. Самый информативный индикатор запасов железа в организме, основная форма депонированного железа. В физиологических условиях метаболизма железа ферритин играет важную роль в поддержании железа в растворимой, нетоксичной и биологически полезной форме. Во время физической нагрузки снижение уровня ферритина свидетельствует о мобилизации железа для синтеза гемоглобина, выраженное снижение – о наличии скрытой железодифицитной анемии. Повышенный уровень сывороточного ферритина отражает не только количество железа в организме, но и является проявлением острофазного ответа на воспалительный процесс. Тем не менее, если у пациента действительно имеется дефицит железа, острофазное повышение его уровня не бывает значительным.
Трансферин. Плазменный белок, гликопротеин — основной переносчик железа. Синтез трансферрина осуществляется в печени и зависит от функционального состояния печени, от потребности в железе и резервов железа в организме. Трансферрин участвует в транспорте железа от места его всасывания (тонкая кишка) до места его использования или хранения (костный мозг, печень, селезенка). При снижении концентрации железа синтез трансферррина возрастает. Снижение процента насыщения трансферрина железом (следствие снижения концентрации железа и роста концентрации трансферрина) указывает на анемию, обусловленную недостатком поступления железа. Длительная интенсивная ФН может привести к увеличению содержания этого транспортного белка в крови. У нетренированных спортсменов ФН может вызвать снижение его уровня.
Миоглобин. В саркоплазме скелетных и сердечной мышц находится высокоспециализированный белок, выполняющий функцию транспорта кислорода подобно гемоглобину. Под влиянием физических нагрузок, при патологических состояниях организма он может выходить из мышц в кровь, что приводит к повышению его содержания в крови и появлению в моче (миоглобинурия). Количество миоглобина в крови зависит от объема выполненной физической нагрузки, а также от степени тренированности спортсмена. Поэтому данный показатель может быть использован для диагностики функционального состояния работающих скелетных мышц.
Актин. Содержание актина в скелетных мышцах в качестве структурного и сократительного белка существенно увеличивается в процессе тренировки. По его содержанию в мышцах можно было бы контролировать развитие скоростно-силовых качеств спортсмена при тренировке, однако определение его содержания в мышцах связано с большими методическими затруднениями. Тем не менее, после выполненных физических нагрузок отмечается появление актина в крови, что свидетельствует о разрушении либо обновлении миофибриллярных структур скелетных мышц.
Белки свертывающей системы крови. «Возраст человека — есть возраст его сосудов» (Демокрит) и данной точки зрения придерживаются большинство современных исследователей. Поэтому весьма актуальным является вопрос стандартизации гемостазиологических критериев утомляемости и оценки степени ФН по оценке эффективности микроциркуляции в организме. Гетерохронность процесса утомления и восстановления подразумевает неравномерность темпов утомляемости отдельных систем человека. Система гемостаза является в филогенетическом смысле наиболее древней и отражает генерализованные изменения, происходящие на уровне целостного организма. Она является наиболее мобильной системой и высокочувствительна к любым нарушениям во внутренней среде организма. Для изучения микроциркуляции и гемостазиограммы определяют уровень фибриногена (ФГ), число тромбоцитов (Тг), активированное парциальное тромбопластиновое время (АПТВ), фибринолитическую активность (ФА), концентрацию растворимых фибринмономерных комплексов (РФМК), уровень антитромбина III (ATIII).
Общий белок. Он определяет физико — химические свойства крови- плотность, вязкость, онкотическое давление. Белки плазмы являются основными траспортными белкамим. Альбумины и глобулины. Это низкомолекулярные основные белки плазмы крови. Они выполняют разнообразные функции .в организме: входят в состав иммунной системы, защищают организм от инфекций, участвуют в поддержании рН крови, транспортируют различные органические и неорганические вещества, используются для построения других веществ. Количественное соотношение их в сыворотке крови в норме относительно постоянно и отражает состояние здоровья человека. Соотношение этих белков изменяется при утомлении, многих заболеваниях и может использоваться в спортивной медицине как диагностический показатель состояния здоровья.
Альбумины — самая однородная фракция белков плазмы. Основная их функция заключается в поддержании онкотического давления. Кроме того большая поверхность молекул альбумина играет существенную роль в переносе жирных кислот, билирубина, солей желчных кислот. Альбумины частично связывают значительную часть ионов кальция. После выполнения физической нагрузки концентрация белка в сыворотке крови, взятой натощак не изменяется. Альфа-глобулины — фракция белков, включающая гликопротеиды. Основная функция — перенос углеводородов, так же транспортные белки для гормонов, витаминов и микроэлементов. Осуществляют транспорт липидов (триглицеридов, фосфолипидов, холестерина. После выполнения нагрузки спортсменами концентрация альфа-глобулинов в крови, взятой натощак снижается по сравнению с уровнем покоя. Бета-глобулины — фракция белков крови участвующая в транспорте фосфолипидов, холестерина, стероидных гормонов, катионов, осуществляет перенос железа кровью. После выполнения спортсменами ФН концентрация бета-глобулинов в крови заметно увеличивается. Гамма-глобулины. В эту фракцию входят различные антитела. Основная функция иммуноглобулинов – защитная. Содержание гамма-глобулинов в сыворотке крови после физической нагрузки уменьшается.
Аммиак. Гипоперфузия скелетных мышц при ФН приводит к клеточной гипоксии, что наряду с другими факторами обусловливает симптомы утомляемости. Мышечная утомляемость — неспособность мышц поддерживать мышечное сокращение заданной интенсивности — связана с избытком аммиака, который усиливает анаэробный гликолиз, блокируя выход молочной кислоты. Повышение уровня аммиака и ацидоз лежат в основе метаболических нарушений при мышечной утомляемости. Причиной последней являются нарушения митохондриального метаболизма, усиление катаболизма белковых структур. Накопление аммиака стимулирует гликолиз путем блокирования аэробного использования пирувата и повторного запуска глюконеогенеза, что приводит к избыточному образованию лактата. Для указанного процесса, представляющего порочный круг, используется термин «метаболическая смерть». Накопление молочной кислоты и ацидоз приводят к гликолизу и «параличу» энергетических процессов. Ион аммония, влияя на метаболизм, стимулирует гиперпноэ, что усугубляет утомление. Снижение сократительной способности мышц сопровождается повышением уровня аммиака в крови и клетке. Усиленный ацидоз и чрезмерно высокий уровень аммиака не позволяют сохранять структуру клетки. Следствием этого является повреждение миофибрилл. В действительности имеет место усиленный катаболизм мышечных белков, затрагивающий скелетную мускулатуру. Это может быть измерено по выделению с мочой 3-метил-гистидина, специфического метаболита мышечных белков. В результате перетренировки возникает истощение резервов глюкозы и липидов, связанное с экстремальным кислотно-основным состоянием. Усиленный ацидоз и чрезмерно высокий уровень аммиака не позволяют сохранять структуру клетки. Гипераммониемия является признаком нарушения метаболизма в мышце и связана с состоянием утомления.
Мочевина. При усиленном распаде тканевых белков, избыточном поступлении в организм аминокислот в печени в процессе связывания токсического для организма человека аммиака (МН3) синтезируется нетоксическое азотсодержащее вещество — мочевина. Из печени мочевина поступает в кровь и выводится с мочой. Концентрация мочевины в норме в крови каждого взрослого человека индивидуальна. Она может увеличиваться при значительном поступлении белков с пищей, при нарушении выделительной функции почек, а также после выполнения длительной физической работы за счет усиления катаболизма белков. В практике спорта этот показатель широко используется при оценке переносимости спортсменом тренировочных и соревновательных физических нагрузок, хода тренировочных занятий и процессов восстановления организма. Для получения объективной информации концентрацию мочевины определяют на следующий день после тренировки утром натощак. Если выполненная физическая нагрузка адекватна функциональным возможностям организма и произошло относительно быстрое восстановление метаболизма, то содержание мочевины в крови утром натощак возвращается к норме. Связано это с уравновешиванием скорости синтеза и распада белков в тканях организма, что свидетельствует о его восстановлении. Если содержание мочевины на следующее утро остается выше нормы, то это свидетельствует о недовосстановлении организма либо развитии его утомления.
Обнаружение белка в моче. У здорового человека белок в моче отсутствует. Появление его (протеинурия) отмечается при заболевании почек (нефрозы), поражении мочевых путей, а также при избыточном поступлении белков с пищей или после мышечной деятельности анаэробной направленности. Это связано с нарушением проницаемости клеточных мембран почек из-за закисления среды организма и выхода белков плазмы в мочу. По наличию определенной концентрации белка в моче после выполнения физической работы судят о ее мощности. Так, при работе в зоне большой мощности она составляет 0,5 %, при работе в зоне субмаксимальной мощности может достигать 1,5 %.
Креатинин. Это вещество образуется в мышцах в процессе распада креатинфосфата. Суточное выделение его с мочой относительно постоянно для данного человека и зависит от мышечной массы тела. По содержанию креатинина в моче можно косвенно оценить скорость креатинфосфокиназной реакции, а также содержание мышечной массы тела. По количеству креатинина, выделяемого с мочой, определяют содержание тощей мышечной массы тела согласно следующей формуле:
тощая масса тела = 0,0291 х креатинин мочи (мг • сут~1) + 7,38.
Креатин. Креатин — это вещество, которое синтезируется в печени, поджелудочной железе и почках из аминокислот аргинина, глицина и метионина. Образуется из фосфокреатина ферментом креатинкиназой. Наличие такого энергетического запаса сохраняет уровень АТФ/АДФ в тех клетках, где необходимы высокие концентрации АТФ. Фосфокреатинкиназная система работает в клетке как внутриклеточная система передача энергии от тех мест, где энергия запасается в виде АТФ (митохондрия и реакции гликолиза в цитоплазме) к тем местам, где требуется энергия (миофибриллы в случае мышечного сокращения). Особенно большое количество креатина содержится в мышечной ткани, где он играет важную роль в процессах энергетического обмена. Тяжелый, высокоинтенсивный тренинг приводит к дефициту фосфоркреатина. Именно этим объясняется физическое утомление, которое нарастает от упражнения к упражнению и достигает пика к концу тренировки. Обнаружение его в моче может использоваться как тест для выявления перетренировки и патологических изменений в мышцах. Увеличение концентрации креатина в эритроцитах является специфическим признаком гипоксии любого происхождения и свидетельствует об увеличении числа молодых клеток, т.е. о стимуляции эритропоэза (в молодых эритроцитах его содержание в 6-8 раз превышает таковое в старых).
Аминокислоты. Анализ аминокислот (мочи и плазмы крови) является незаменимым средством оценки достаточности и степени усвоения пищевого белка, а также метаболического дисбаланса, лежащего в основе многих хронических нарушений при утомляемости после ФН. Жизнь без аминокислот невозможна. В свободной форме или в связанном виде как пептиды они играют важную роль в таких процессах, как нейротрансмиттерная функция, регуляция рН, метаболизм холестерина, контроль боли, детоксикация и контроль воспалительных процессов. Аминокислоты являются строительными блоками всех гормонов и структурных тканей организма. Поскольку все эти соединения получаются или строятся из аминокислот, то оценка поступления «незаменимых» аминокислот с пищей, их достаточности, правильности баланса между ними и активностью ферментов, которые превращают их в гормоны, имеет основополагающее значение для выяснения исходной причины многих хронических нарушений. Анализ аминокислот, позволяет получить информацию о широком спектре нарушений обмена веществ и питания, включая белковые отклонения, хроническую усталость.
Показатели кислотно-основного состояния (КОС) организма. В процессе интенсивной мышечной деятельности в мышцах образуется большое количество молочной и пировиноградной кислот, которые диффундируют в кровь и могут вызывать метаболический ацидоз организма, что приводит к утомлению мышц и сопровождается болями в мышцах, головокружением, тошнотой. Такие метаболические изменения связаны с истощением буферных резервов организма. Поскольку состояние буферных систем организма имеет важное значение в проявлении высокой физической работоспособности, в спортивной диагностике используются показатели КОС — рН крови, ВЕ избыток оснований, или щелочной резерв, рСО2 — парциальное давление углекислого газа, ВВ — буферные основания цельной крови. Показатели КОС отражают не только изменения в буферных системах крови, но и состояние дыхательной и выделительной систем организма в том числе после ФН. Существует корреляционная зависимость между динамикой содержания лактата в крови и изменением рН крови. По изменению показателей КОС при мышечной деятельности можно контролировать реакцию организма на физическую нагрузку. Наиболее информативным показателем КОС является величина ВЕ — щелочной резерв, который увеличивается с повышением квалификации спортсменов, особенно специализирующихся в скоростно-силовых видах спорта.
Активная реакция мочи (рН) находится в прямой зависимости от кислотно-основного состояния организма. При метаболическом ацидозе кислотность мочи увеличивается до рН 5, а при метаболическом алкалозе снижается до рН 7.
Регуляторы обмена веществ.
Ферменты. Особый интерес в спортивной диагностике представляют тканевые ферменты, которые при различных функциональных состояниях организма поступают в кровь из скелетных мышц и других тканей. Такие ферменты называются клеточными, или индикаторными. К ним относятся альдолаза, каталаза, лактатдегидрогеназа, креатинкиназа. Повышение в крови индикаторных ферментов или их отдельных изоформ связано с нарушением проницаемости клеточных мембран тканей и может использоваться при биохимическом контроле за функциональным состоянием спортсмена. Результатом повреждения клеточной мембраны является выход в кровь цитоплазматических (миоглобин, аспартатаминотрансфераза) и структурных (тропомиозин) белков скелетной мышцы. Диагностика микроповреждений мышечной ткани (ММТ) базируется на измерении активности в плазме крови саркоплазматических ферментов (креатинкиназы лактатдегидрогеназы). Повышение их активности в плазме крови отражает значительное изменение проницаемости мембранных структур миоцита, вплоть до его полного разрушения. Данный факт отражает адаптацию организма спортсмена к ФН высокой интенсивности. При постановке диагноза микроповреждения используется комбинация из биологических и клинических параметров — например, активность ЛДГ и КФК в плазме, концентрация миоглобина и малондиальдегида, уровень лейкоцитов, а также физиологические параметры мышцы.
Появление в крови ферментов процессов биологического окисления веществ альдолазы (фермент гликолиза) и каталазы (фермент, осуществляющий восстановление перекисей водорода) после физических нагрузок является показателем неадекватности физической нагрузки, развития утомления, а скорость их исчезновения свидетельствует о скорости восстановления организма. Если физическая нагрузка вызывает значительный выход ферментов в кровь из тканей и они долго сохраняются в ней в период отдыха, это свидетельствует о невысоком уровне тренированности спортсмена, а, возможно, и о предпатологическом состоянии организма.
Гормоны. К показателям функциональной активности организма можно отнести: особенности метаболизма в целом, активность ряда ферментов, количественная секреция многих гормонов. Поэтому важно исследовать взаимосвязь этих показателей с ФН. Неоспоримо влияние мышечной нагрузки на состояние внутренней среды организма. В крови могут определяться более 20 различных гормонов, регулирующих разные звенья обмена веществ. Величина изменения содержания гормонов в крови зависит от мощности и длительности выполняемых нагрузок, а также от степени тренированности спортсмена. При работе одинаковой мощности у более тренированных спортсменов наблюдаются менее значительные изменения этих показателей в крови. Кроме того, по изменению содержания гормонов в крови можно судить об адаптации организма к физическим нагрузкам, интенсивности регулируемых ими метаболических процессов, развитии процессов утомления, применении анаболических стероидов и других гормонов.
Физическая нагрузка сама по себе значительно увеличивает уровень многих гормонов в крови и не только во время выполнения самого упражнения. После начала выполнения непрерывного упражнения, например, субмаксимальной мощности, в течение первых 3-10 минут в крови уровень многих метаболитов и гормонов изменяется совершенно непредсказуемо. Этот период «врабатывания» вызывает некоторую десинхронизацию в уровне регуляторных факторов. Однако некоторые закономерности таких изменений все же существуют. Освобождение гормонов в кровоток при физической нагрузке представляет собой набор каскадных реакций. Упрощенная схема этого процесса может выглядеть примерно так: физическая нагрузка — гипоталамус, гипофиз — высвобождение тропных гормонов и эндорфинов — железы внутренней секреции — высвобождение гормонов — клетки и ткани организма.
Профиль гормонов служит важным средством выявления скрытых биохимических нарушений, лежащих в основе хронической усталости. Изучение уровня кортизола в крови целесообразно для оценки мобилизационных резервов организма. Он рассматривается как основной «гормон стресса», и увеличение его концентрации в крови является ответной реакцией организма на физические, физиологические и психологические нагрузки. Избыточные количества кортизола могут негативно влиять на костную и мышечную ткань, сердечно-сосудистую функцию, иммунную защиту, функцию щитовидной железы, контроль массы тела, сон, регуляцию уровня глюкозы и ускорять процесс старения. Высокий уровень кортизола после тренировки характеризуется недовосстановлением организма спортсменов после предшествующей нагрузки.
В спортивной медицине для выявления утомления обычно определяют содержание гормонов симпато-адреналовой системы (адреналина, норадреналин, серотонин) в крови и моче. Эти гормоны отвечают за степень напряжения адаптационных изменений в организме. При неадекватных функциональному состоянию организма физических нагрузках наблюдается снижение уровня не только гормонов, но и предшественников их синтеза (дофамин) в моче, что связано с исчерпанием биосинтетических резервов эндокринных желез и указывает на перенапряжение регуляторных функций организма контролирующих адаптационные процессы.
Гормон роста (соматотропный гормон), инсулинподобный фактор роста (Соматомедин С). Основные физиологические эффекты гормона роста: ускорение роста тканей тела — специфическое действие; усиление синтеза белков и повышение проницаемости мембран клеток для аминокислот; ускорение расщепление глюкозы и окисление жиров. Его эффекты проявляются в облегчении утилизации глюкозы тканями, активации в них синтеза белка и жира, повышения транспорта аминокислот через клеточную мембрану. Эти эффекты характерны для кратковременного действия соматотропина. Интенсивная ФН приводит к снижению концентрации гормона в сыворотке крови, взятой натощак. При увеличении продолжительности ФН в кровотоке концентрация соматотропина увеличивается.
Паратгормон и кальцитонин принимают участие в регуляции содержания кальция и фосфатов. Паратгормон осуществляет действие, активируя аденилатциклазу и стимулируя образование цАМФ внутри клетки. Основное назначение инсулина — повышает потребление глюкозы тканями, вследствие чего понижается содержание сахара в крови. Он влияет на все виды обмена веществ, стимулирует транспорт веществ через клеточные мембраны, тормозит липолиз и активирует липогенез. Снижение концентрации инсулина в крови под влиянием мышечной работы, становится значительным уже через 15-20 минут после физической нагрузки. Причина изменения уровня инсулина в крови во время работы заключается в угнетении его секреции, что обуславливает увеличение выработки глюкозы. Концентрация гормона в крови зависит от скорости окисления глюкозы и от уровня других гормонов участвующих в регуляции содержания. После выполнения физической нагрузки спортсменами концентрация гормона в крови, взятой натощак, снижается.
Паратгормон и кальцитонин необходимы для обеспечения работоспособности, и при мышечной работе имеет место повышение уровня кальцитонина и паратгормона в крови. Наиболее значительно различалось содержание кальцитонина в плазме крови. Занятия спортом оказали значительное влияние на исследуемые вещества. Скорее всего это связано с адаптацией спортсменов к высокому уровню двигательной активности.
Тестостерон. Тестостерон оказывает анаболические эффекты на мышечную ткань, способствует созреванию костной ткани, стимулирует образование кожного сала железами кожи, участвует в регуляции синтеза липопротеидов печенью, модулирует синтез b-эндорфинов («гормонов радости»), инсулина. У мужчин обеспечивает формирование половой системы по мужскому типу, развитие мужских вторичных половых признаков в пубертатном периоде, активирует половое влечение, сперматогенез и потенцию, отвечает за психофизиологические особенности полового поведения.
Спортивным врачам очень хорошо известно, что в нашем современном промышленном обществе существуют две крайности: люди, которые с чрезмерным энтузиазмом устремляются в спорт и в свое свободное время настолько же нацелены на достижение результатов, как и на работе; и люди, которые занимаются спортом слишком мало. Обе крайности отрицательно сказываются на уровне тестостерона. Изнуряющие физические нагрузки (например, марафон) понижают уровень тестостерона почти в той же степени, что и отсутствие физической активности. В наше время проблема заключается в перегрузках, возникающих в результате интенсивных спортивных тренировок, что, как представляется, влечет за собой значительное снижение уровня тестостерона в крови.
Максимальная физическая нагрузка приводит к увеличению концентрации в крови адренокортикотропного гормона, соматотропного гормона, кортизола и трийодтиронина и снижению содержания инсулина. При длительной ФН концентрации кортизола и индекса тестостерон/кортизол снижается.
Витамины. Выявление витаминов в моче входит в диагностический комплекс характеристики состояния здоровья спортсменов, их физической работоспособности. В практике спорта чаще всего выявляют обеспеченность организма водорастворимыми витаминами, особенно витамином С. В моче витамины появляются при достаточном обеспечении ими организма. Данные многочисленных исследований свидетельствуют о недостаточной обеспеченности многих спортсменов витаминами, поэтому контроль их содержания в организме позволит своевременно скорректировать рацион питания или назначить дополнительную витаминизацию путем приема специальных поливитаминных комплексов.
Минеральные вещества. В мышцах образуется неорганический фосфат в виде фосфорной кислоты (Н3Р04) при реакциях перефосфорилирования в креатинфосфокиназном механизме синтеза АТФ и других процессах. По изменению его концентрации в крови можно судить о мощности креатинфосфокиназного механизма энергообеспечения у спортсменов, а также об уровне тренированности, так как прирост неорганического фосфата в крови спортсменов высокой квалификации при выполнении анаэробной физической работы больше, чем в крови менее квалифицированных спортсменов.
Железо. Основные функции железа
1. транспорт электронов (цитохромы, железосеропротеиды);
2. транспорт и депонирование кислорода (миоглобин, гемоглобин);
3. участие в формировании активных центров окислительно-восстановительных ферментов (оксидазы, гидроксилазы, СОД);
4. активация перекисного окисления, предварительно подготовленного ионами меди;
5. транспорт и депонирование железа (трансферрин, ферритин, гемосидерин, сидерохромы, лактоферрин);
6. участие в синтезе ДНК, делении клеток;
7. участие в синтезе простагландинов, тромбоксанов, лейкотриенов и коллагена;
8. участие в метаболизме гормонов мозгового вещества надпочечников;
9. участие в метаболизме альдегидов, ксантина;
10. участие в катаболизме ароматических аминокислот, пероксидов;
11. лекарственная детоксикация
При дефиците Fe отмечается гипохромная анемия, миоглобиндефицитная кардиопатия и атония скелетных мышц, воспалительные и атрофические изменения слизистой рта, носа, эзофагопатия, хронический гастродуоденит а также иммунодефицитные состояния. Избыток Fe, в первую очередь, может оказывать токсическое влияние на печень, селезенку, головной мозг, усиливать воспалительные процессы в организме человека. Хроническая алкогольная интоксикация может приводить к накоплению Fe в организме.
Калий — важнейший внутриклеточный элемент-электролит и активатор функций ряда ферментов. Калий особенно необходим для «питания» клеток организма, деятельности мышц, в том числе миокарда, поддержания водно-солевого баланса организма, работы нейроэндокринной системы. Это — основной элемент в каждой живой клетке. Внутриклеточный калий находится в постоянном равновесии с малым количеством того, который остается снаружи клетки. Это соотношение обеспечивает прохождение электрических нервных импульсов, контролирует сокращения мышцы, обеспечивает стабильность артериального давления. Калий улучшает снабжение мозга кислородом. Как эмоциональный, так и физический стресс могут также привести к дефициту калия. Калий, натрий и хлор теряются с потом, поэтому у спортсменов может возникать потребность восполнения этих элементов специальными напитками и препаратами. Злоупотребление алкоголем ведет к потере калия
Основные функции калия
1. регулирует внутриклеточный обмен, обмен воды и солей;
2. поддерживает осмотическое давление и кислотно-щелочное состояние организма;
3. нормализует деятельность мышц;
4. участвует в проведении нервных импульсов к мышцам;
5. способствует выведению из организма воды и натрия;
6. активирует ряд ферментов и участвует в важнейших метаболических процессах (энергообразование, синтез гликогена, белков, гликопротеинов);
7. участвует в регуляции процесса выделения инсулина клетками поджелудочной железы;
8. поддерживает чувствительность гладкомышечных клеток к сосудосуживающему действию ангиотензина.
Причины дефицита калия у спортсменов – обильное потоотделение, клинические симптомы – слабость и утомление, физическое истощение, переутомление
Кальций — это макроэлемент, играющий важную роль в функционировании мышечной ткани, миокарда, нервной системы, кожи и, особенно, костной ткани при его дефиците. Кальций имеет крайне важное значение для здоровья человека, он управляет многочисленными процессами жизнедеятельности всех основных систем организма. Са преимущественно находится в костях, обеспечивая опорную функцию и защитную роль скелета для внутренних органов. 1 % Са в ионизированной форме циркулирует в крови и межклеточной жидкости, участвуя в регуляции нервно-мышечной проводимости, сосудистого тонуса, продукции гормонов, проницаемости капилляров, в обеспечении репродуктивной функции, свертываемости крови, препятствуя депонированию в организме токсинов, тяжелых металлов и радиоактивных элементов
Хром. При недостаточности хрома в организме у спортсменов нарушаются процессы высшей нервной деятельности (появление беспокойства, утомляемости, бессонницы, головных болей).
Цинк — Он управляет сокращаемостью мышц, необходим для синтеза белка (печенью), пищеварительных ферментов и инсулина (поджелудочной железой), очищения организма.
Магний. Магний, наряду с калием, является основным внутриклеточным элементом — активизирует ферменты, регулирующие углеводный обмен, стимулирует образование белков, регулирует хранение и высвобождение энергии в АТФ, снижает возбуждение в нервных клетках, расслабляет сердечную мышцу. У спортсменов снижение уровня магния в крови является следствием перетренировки и утомления. Недостаток предрасполагает к развитию заболеваний сердечно-сосудистой системы, гипертонической болезни, уролитиаза, судорог.
Биохимический контроль развития систем энергообеспечения организма при мышечной деятельности.
Спортивный результат в определенной степени лимитируется уровнем развития механизмов энергообеспечения организма. Поэтому в практике спорта проводится контроль мощности, емкости и эффективности анаэробных и аэробных механизмов энергообразования в процессе тренировки.
Для оценки мощности и емкости креатинфосфокиназного механизма энергообразования можно использовать показатели количества креатинфосфата и активности креатинфосфокиназы в крови. В тренированном организме эти показатели значительно выше, что свидетельствует о повышении возможностей креатинфосфокиназного (алактатного) механизма энергообразования. Степень подклю-чения креатинфосфокиназного механизма при выполнении физических нагрузок можно оценить по увеличению в крови содержания продуктов обмена КрФ в мышцах (креатина, креатинина и неорганического фосфата) и изменению их содержания в моче
Для характеристики гликолитического механизма энергообразования часто используют величину максимального накопления лактата в артериальной крови при максимальных физических нагрузках, а также значение рН крови и показатели КОС, содержание глюкозы в крови, активность ферментов лактатдегидрогеназы, фосфорилазы. О повышении возможностей гликолитического (лактатного) энергообразования у спортсменов свидетельствует более поздний выход на максимальное количество лактата в крови при предельных физических нагрузках, а также более высокий его уровень. Увеличение емкости гликолиза сопровождается увеличением запасов гликогена в скелетных мышцах, особенно в быстрых волокнах, а также повышением активности гликолитических ферментов.
Для оценки мощности аэробного механизма энергообразования чаще всего используются уровень максимального потребления кислорода (МПК или ИЭ2тах) и показатель кислородтранспортной системы крови – концентрация гемоглобина. Эффективность аэробного механизма энергообразования зависит от скорости утилизации кислорода митохондриями, что связано прежде всего с активностью и количеством ферментов окислительного фосфорилирования, количеством митохондрий, а также от доли жиров при энергообразовании. Под влиянием интенсивной тренировки аэробной направленности увеличивается эффективность аэробного механизма за счет увеличения скорости окисления жиров и увеличения их роли в энергообеспечении работы. При однократных и систематических ФН с аэробной направленностью метаболических процессов наблюдается усиление липидного метаболизма как жировой ткани, так и скелетных мышц. Повышение интенсивности аэробных ФН приводит к увеличению мобилизации внутримышечных триглицеридов и утилизации жирных кислот в работающих мышцах за счет активизации процессов их транспорта.
Биохимический контроль за уровнем тренированности, утомления и восстановления организма футболиста.
Контроль за процессами утомления и восстановления, которые являются неотъемлемыми компонентами спортивной деятельности, необходим для оценки переносимости физической нагрузки и выявления перетренированности, достаточности времени отдыха после физических нагрузок, эффективности средств повышения работоспособности. Сроки восстановления после тяжёлых тренировок не являются строго детерминированными и зависят от характера нагрузки и степени истощения систем организма под её воздействием.
Уровень тренированности оценивается по изменению концентрации лактата в крови при выполнении стандартной либо предельной физической нагрузки для данного контингента спортсменов. О более высоком уровне тренированности свидетельствуют меньшее накопление лактата (по сравнению с нетренированными) при выполнении стандартной нагрузки, что связано с увеличением доли аэробных механизмов в энергообеспечении этой работы; меньшее увеличение содержания лактата в крови при возрастании мощности работы, увеличение скорости утилирации лактата в период восстановления после ФН.
С увеличением уровня тренированности спортсменов увеличивается общая масса крови, что приводит к увеличению концентрации гемоглобина до 160—180 г • л»1 — у мужчин и до 130—150 г • л»1 — у женщин, увеличению скорости утилизации лактата в период восстановления после физических нагрузок.
Утомление, вызванное физическими нагрузками максимальной и субмаксимальной мощности, связано с истощением запасов энергетических субстратов (АТФ, КрФ, гликогена) в тканях, обеспечивающих этот вид работы, и накоплением продуктов их обмена в крови (молочной кислоты, креатина, неорганических фосфатов), поэтому и контролируется по этим показателям. При выполнении продолжительной напряженной работы развитие утомления может выявляться по длительному повышению уровня мочевины в крови после окончания работы, по изменению компонентов иммунной системы крови, а также по снижению содержания гормонов в крови и моче.
Для ранней диагностики перетренированности, скрытой фазы утомления используется контроль за функциональной активностью иммунной системы. Для этого определяют количество и функциональную активность клеток Т- и В-лимфоцитов: Т-лимфоциты обеспечивают процессы клеточного иммунитета и регулируют функцию В-лимфоцитов; В-лимфоциты отвечают за процессы гуморального иммунитета, их функциональная активность определяется по количеству иммуноглобулинов в сыворотке крови.
При подключении иммунологического контроля за функциональным состоянием спортсмена необходимо знать его исходный иммунологический статус с последующим контролем в различные периоды тренировочного цикла. Такой контроль позволит предотвратить срыв адаптационных механизмов, исчерпание иммунной системы и развитие инфекционных заболеваний спортсменов высокой квалификации в периоды тренировки и подготовки к ответственным соревнованиям (особенно при резкой смене климатических зон).
Восстановление организма связано с возобновлением количества израсходованных во время работы энергетических субстратов и других веществ. Их восстановление, а также скорость обменных процессов происходят не одновременно. Знание времени восстановления в организме различных энергетических субстратов играет большую роль в правильном построении тренировочного процесса. Восстановление организма оценивается по изменению количества тех метаболитов углеводного, липидного и белкового обменов в крови или моче, которые существенно изменяются под влиянием тренировочных нагрузок. Из всех показателей углеводного обмена чаще всего исследуется скорость утилизации во время отдыха молочной кислоты, а также липидного обмена — нарастание содержания жирных кислот и кетоновых тел в крови, которые в период отдыха являются главным субстратом аэробного окисления, о чем свидетельствует снижение дыхательного коэффициента. Однако наиболее информативным показателем восстановления организма после мышечной работы является продукт белкового обмена — мочевина. При мышечной деятельности усиливается катаболизм тканевых белков, способствующий повышению уровня мочевины в крови, поэтому нормализация ее содержания в крови свидетельствует о восстановлении синтеза белка в мышцах, а следовательно, и восстановлении организма.
Оценка повреждения мышечной ткани. Скелетные мышцы обеспечивают любую двигательную активность организма. Выполнение данной функции вызывает значительные биохимические и морфологические изменения в ткани скелетных мышц, и чем интенсивнее двигательная активность, тем большие изменения обнаруживаются. Систематические нагрузки способствуют закреплению ряда возникших биохимических изменений, что определяет развитие состояния тренированности скелетных мышц, которое обеспечивает выполнение более высоких ФН. Вместе с тем и тренированные мышцы повреждаются при выполнении ФН, хотя порог повреждения в этом случае выше по сравнению с нетренированными мышцами.
Начальная, инициирующая фаза повреждения — механическая, за которой следует вторичное метаболическое или биохимическое повреждение, достигающее максимума на 1-3-й дни после повреждающего сокращения, что хорошо совпадает с динамикой развития дегенеративного процесса. Повреждения структуры мышц при продолжительных или напряженных ФН сопровождаются появлением усталости. В случае пролонгированных ФН в качестве фактора повреждения мышцы отмечаются гипоксические условия, реперфузия, образование свободных радикалов и повышение лизосомальной активности. Принятым биохимическим показателем повреждения мышц является появление в крови мышечных белков (миоглобин, креатинкиназа — КК, лактатдегидрогеназа, аспартатаминотрансфераза — АсАТ), так и структурных (тропомиозин, миозин) белков мышечной ткани. Обнаружение в крови белков скелетных мышц является доказательством повреждения мышечной ткани при ФН. Механизм повреждения скелетных мышц при ФН включает ряд процессов:
1) Нарушения гомеостаза Са2+, сопровождающиеся повышением внутриклеточной концентрации Са2+, что приводит к активации калпаинов (нелизосомальные цистеиновые протеазы), которые играют важную роль в запуске расщепления белков скелетных мышц, воспалительных изменениях и процессе регенерации;
2) Усиление окислительных процессов, в том числе процесса перекисного окисления липидов (ПОЛ), что приводит к повышению проницаемости мембран миоцитов;
3) Асептическая воспалительная реакция, протекающая с участием лейкоцитов и активацией циклооксигеназы-2;
4) физический разрыв сарколеммы.
В роли одного из важных факторов, инициирующего каскад биохимических реакций, определяющих повреждение мышцы, рассматривают механический стресс. Значение данного фактора в повреждении скелетных мышц подчеркивает уникальность этой ткани, структура которой предназначена для выполнения сократительной функции. Мышцы здорового человека не подвергаются ишемии – приток крови в них достаточен. Вместе с тем высоко интенсивные ФН вызывают сильную метаболичесткую гипоксию мышц, последствия которой после прекращения ФН сходны с реперфузией при ишемии. В развитии повреждения важным оказывается не столько ишемия, сколько последующая реперфузия, поэтому основными маркерами повреждения являются высокий уровень активных форм кислорода (АФК) — инициаторов ПОЛ и воспалительных лейкоцитов — нейтрофилов. В основе реализации этого механизма лежит как локальное усиление свободно-радикальных процессов, так и накопление воспалительных лейкоцитов. Наряду с активацией ПОЛ выявляется снижение активности супероксиддисмутазы – одного из ключевых ферментов антиоксидантной защиты. Наличие достоверных коррелятивных связей между активностью в крови ряда ферментов скелетных мышц (КК, лактатдегидрогеназа) и концентрацией малонового диальдегида — продукта ПОЛ — у футболистов являясь важным фактором модификации клеточных мембран, вызывает изменение их физико-химических свойств, проницаемости, что и определяет выход в циркуляцию мышечных белков. Уже в процессе нагрузки, протекающей в условиях гипоксии, в мышцах развивается комплекс «повреждающих» метаболических реакций. Увеличивается концентрация внутриклеточного Ca2+, что ведет к активации Ca2+ -зависимых протеиназ — калпаинов; вследствие нарушения энергетического обмена истощаются запасы макроэргов в мышечном волокне; развивается ацидоз в связи с продукцией большого количества лактата. По завершении нагрузки в мышцах включаются реакции повреждения следующего эшелона, связанные с активацией окислительных процессов и лейкоцитарной инфильтрацией. Наиболее информативными маркерами мышечного повреждения являются уровень активности КК и концентрация миоглобина в плазме/сыворотке крови.
Повреждения, возникающие в скелетных мышцах при выполнении ФН высокой интенсивности и длительности, могут быть уменьшены с помощью адекватной фармакологической поддержки, а также соответствующей физиотерапевтической подготовки мышц к выполнению нагрузки. Ускорения восстановления повреждений можно добиться также, применяя фармакологическую поддержку, наряду с известными физиотерапевтическими мероприятиями. Учитывая сведения о механизмах повреждения скелетных мышц при выполнении ФН высокой интенсивности, с целью заблаговременной фармакологической поддержки скелетных мышц можно использовать различные комплексные препараты антиоксидантов и возможно определенные нестероидные противовоспалительные препараты. Как те, так и другие применяются спортсменами, однако на наш взгляд очень важно определить тактику применения препаратов, основываясь на ясном понимании процессов, происходящих в мышцах при ФН и в период реституции. С этих позиций наиболее разумно поддержку с использованием антиоксидантов начинать хотя бы за несколько дней до соревнований и не прекращать в процессе соревнований. Противовоспалительные препараты следует использовать, по-видимому, перед нагрузкой, а возможно и сразу после нее. Использование противовоспалительных препаратов может помочь подавить воспалительный процесс, в частности тот его этап, который связан с формированием локального структурно-метаболического фона, определяющего приток лейкоцитов.
Биохимические маркеры перенапряжения и тренированности.
Перенапряжение мышечной ткани — одна из наиболее частых проблем, с которыми сталкиваются спортсмены при выполнении физической нагрузки высокой интенсивности. На сегодняшний день молекулярная диагностика этого феномена, в основном, базируется на измерении активности в плазме крови различных саркоплазматических ферментов (креатинкиназы (КФК) и лактатдегидрогеназы (ЛДГ)). В норме эти ферменты проникают за пределы клеточной мембраны в незначительных количествах, и повышение их активности в плазме крови отражает значительное изменение проницаемости мембранных структур миоцита, вплоть до его полного разрушения. У спортсменов активность КФК и ЛДГ значительно превосходит таковую у обычных людей. Данный факт отражает адаптацию организма спортсмена к ФН высокой интенсивности. Если у нетренированного человека при повреждении скелетной мускулатуры уровни КФК и ЛДГ растут на порядок, то у спортсменов они, зачастую, остаются неизменными. При перенапряжении мышечной ткани лучше использовать комбинацию из биологических и клинических параметров — например, активность ЛДГ и КФК в плазме, концентрация миоглобина и малондиальдегида, уровень лейкоцитов, а также физиологические параметры мышцы. Высокая активность КФК и высокий уровень малондиальдегида в сыворотке крови хорошо отражают перенапряжение мышечной ткани.
Оценка функционального состояния организма и готовности к повышенным нагрузкам.
При оценке адекватности физических нагрузок в период интенсивных занятий спортом стоит задача поиска объективных маркёров состояния мышечной ткани и др. систем организма. Мы предлагаем в качестве таких критериев использовать биохимические показатели работы основных органов: В первую очередь обращаем внимание на состояние мышечной системы и сердца:
— общая КФК, как правило, повышается при интенсивных занятиях (к повышению уровня фермента приводит недостаточность кровоснабжения мышц). Однако необходимо следить за тем, чтобы это повышение было умеренным. Кроме этого, за повышением общего уровня КФК за счет напряжения скелетной мускулатуры, можно пропустить начало разрушения сердечной мышцы – обязательно проверяем миокардиальную фракцию КФК — МВ.
— ЛДГ и АСТ – саркоплазматические ферменты помогут оценить состояние сердечной мышцы и скелетной мускулатуры.
— Миоглобин обеспечивает транспорт и хранение кислорода в поперечно-полосатой мускулатуре. При повреждении мышц происходит высвобождение миоглобина в сыворотку крови и появление его в моче. Концентрация его в сыворотке пропорциональна мышечной массе, поэтому у мужчин базовый уровень миоглобина выше (как правило). Определение миоглобина может использоваться для определения уровня подготовки атлета – выход в сыворотку миоглобина задерживается у тренированных спортсменов и увеличен у потерявших спортивную форму. Значительное увеличение концентрации миоглобина наблюдается при деструкции клеток скелетной мускулатуры и при перенапряжении мышц.
— При выявлении повышенных уровней КФК-МВ или значительном скачке концентрации миоглобина на фоне тренировок необходимо срочно назначить тест на Тропонин (количественный) для исключения развития инфаркта миокарда. Корме этого, мы предлагаем для диагностики хронической сердечной недостаточности определять уровень BNP (натрий-уретический гормон, вырабатываемый сердечной мышцей).
— Исследовать электролитный баланс (Na, K, Cl, Ca++, Mg).
— Интенсивная работа скелетных мышц (особенно в начале занятий у нетренированных лиц или после длительного перерыва) сопровождается накоплением молочной кислоты (лактата) в мышцах. Повышение кислотности за счет молочной кислоты (лактоацидоз) может происходить из-за тканевой гипоксии и проявлять себя в виде мышечных болей. Следовательно, необходим контроль за уровнем лактата и кислотно-основным равновесием (газы крови);
— Повышение потребления кислорода мышцами отражается на интенсивности синтеза и распада эритроцитов. Чтобы оценить состояние эритропоэза и контролировать гемолиз необходим мониторинг уровня гемоглобина и гематокрита, а также гаптоглобина и билирубина (прямого и общего) – показателей повышенного гемолиза. Если обнаруживаются какие-либо сдвиги в этих показателях – назначается исследование обмена железа, витамина В12 и фолатов (чтобы проверить, хватает ли организму витаминов и микроэлементов для поддержания интенсивного уровня эритропоэза.
Виды и организация биохимического контроля у футболистов.
Определение биохимических показателей обмена веществ позволяет решать следующие задачи
— комплексного обследования: контроль за функциональным состоянием организма спортсмена, которое отражает эффективность и рациональность выполняемой индивидуальной тренировочной программы, —
— наблюдение за адаптационными изменениями основных энергетических систем и функциональной перестройкой организма в процессе тренировки,
— диагностика предпатологических и патологических изменений метаболизма спортсменов.
Биохимический контроль позволяет также решать такие частные задачи, как выявление реакции организма на физические нагрузки, оценка уровня тренированности, адекватности применения фармакологических и других восстанавливающих средств, роли энергетических метаболических систем в мышечной деятельности, воздействия климатических факторов и др. В связи с этим в практике спорта используется биохимический контроль на различных этапах подготовки спортсменов.
В годичном тренировочном цикле подготовки квалифицированных футболистов выделяют разные виды биохимического контроля:
• текущие обследования (ТО), проводимые повседневно в соответствии с планом подготовки;
• этапные комплексные обследования (ЭКО), проводимые 3—4 раза
в год;
• углубленные комплексные обследования (УКО), проводимые 2 раза
в год;
• обследование соревновательной деятельности (ОСД).
На основании текущих обследований определяют функциональное состояние спортсмена — одно из основных показателей тренированности, оценивают уровень срочного и отставленного тренировочного эффекта физических нагрузок, проводят коррекцию физических нагрузок в ходе тренировок.
В процессе этапных и углубленных комплексных обследований футболистов с помощью биохимических показателей можно оценить кумулятивный тренировочный эффект, причем биохимический контроль дает тренеру, педагогу или врачу быструю и достаточно объективную информацию о росте тренированности и функциональных системах организма, а также других адаптационных изменениях.
При организации и проведении биохимического обследования особое внимание уделяется выбору тестирующих биохимических показателей: они должны быть надежными либо воспроизводимыми, повторяющимися при многократном контрольном обследовании, информативными, отражающими сущность изучаемого процесса, а также валидными либо взаимосвязанными со спортивными результатами.
В каждом конкретном случае определяются разные тестирующие биохимические показатели обмена веществ, поскольку в процессе мышечной деятельности по-разному изменяются отдельные звенья метаболизма. Первостепенное значение приобретают показатели тех звеньев обмена веществ, которые являются основными в обеспечении спортивной работоспособности в данном виде спорта.
Немаловажное значение в биохимическом обследовании имеют используемые методы определения показателей метаболизма, их точность и достоверность. В настоящее время в практике спорта широко применяются лабораторные методы определения многих (около 60) различных биохимических показателей в плазме крови. Одни и те же биохимические методы и показатели могут быть использованы для решения различных задач. Так, например, определение содержания лактата в крови используется при оценке уровня тренированности, направленности и эффективности применяемого упражнения, а также при отборе лиц для занятий отдельными видами спорта.
В зависимости от решаемых задач изменяются условия проведения биохимических исследований. Поскольку многие биохимические показатели у тренированного и не тренированного организма в состоянии относительного покоя существенно не различаются, для выявления их особенностей проводят обследование в состоянии покоя утром натощак (физиологическая норма), в динамике физической нагрузки либо сразу после нее, а также в разные периоды восстановления.
При выборе биохимических показателей следует учитывать, что реакция организма человека на физическую нагрузку может зависеть от факторов, непосредственно не связанных с уровнем тренированности, в частности от вида тренировки, квалификации спортсмена, а также от окружающей обстановки, температуры среды, времени суток и др. Более низкая работоспособность наблюдается при повышенной температуре среды, а также в утреннее и вечернее время. К тестированию, как и к занятиям, спортом, особенно с максимальными нагрузками, должны допускаться только полностью здоровые футболисты, поэтому врачебный осмотр должен предшествовать другим видам контроля. Контрольное биохимическое тестирование проводится утром натощак после относительного отдыха в течение суток. При этом должны соблюдаться примерно одинаковые условия внешней среды, которые влияют на результаты тестирования.
Для оценки влияния физической нагрузки биохимические исследования проводятся спустя 3-7 минут после тренировки, когда наступают наибольшие изменения в крови. Изменение биохимических показателей под воздействием физических нагрузок зависит от степени тренированности, объема выполненных нагрузок, их интенсивности и анаэробной или аэробной направленности, а также от пола и возраста обследуемых. После стандартной физической нагрузки значительные биохимические сдвиги обнаруживаются у менее тренированных людей, а после максимальных — у высокотренированных. При этом после выполнения специфических для спортсменов нагрузок в условиях соревнования или в виде прикидок в тренированном организме возможны значительные биохимические изменения, которые не характерны для нетренированных людей.
Спектр биохимических маркеров по видам обследования футболистов.
Углубленное медицинское обследование.
Скриннинг, позволяющий «отфильтровать» группу спортсменов, нуждающихся в дообследовании (готовность к сезону):
• ОАК (RBC, HGB, HCT, MCV, MCH, MCHC, RDW + ретикулоциты, PLT)
• ОАМ (рН, плотность, кетоны, соли, белок, глюкоза)
• Коагулограмма (Фг, Пр, Ат111, ТВ. АЧТВ, РКМФ, Д-димер, ФА)
• БАК (мочевина, мочевая кислота, холестерин, липиды, глюкоза, АСТ, АЛТ, креатинин, КФК, КФК MB, ЩФ, ЛДГ, магний, кальций, фосфор, калий, натрий, железо, ферритин, амилаза, белок, альбумин, глобулин и фракции, аминокислоты, СМП, Тропонин –Т, BNP)
• Гормоны (кортизол, тестостерон, инсулин, С-пептид, адреналин, эритропоэтин, гормон роста , Соматомедин С, паратгормон, кальцитонин, ТТГ, св. Т4)
• Инфекции (TORCH, ЗППП)
• Наркотики
• Микроэлементы (цинк, хром, селен)
Этапное медицинское обследование.
• ОАК, ОАМ, БАК
• Коагулогрумма (оценка микроциркуляции)
• Антиоксидантный статус (малоновый диальдегид, супероксиддисмутаза)
• Диагностика анемий (железо, ферритин, трансферин, ОЖСС, Витамин В12, фолиевая кислота)
Контрольное медицинское обследование.
(по усмотрению врача и в зависимости от физической нагрузки и состояния футболиста)
• Гемоглобин, эритроциты
• Мочевина, креатинин, аммиак, молочная кислота
Оценка состояния организма и готовности к повышенным нагрузкам
(обследование футболиста перед заключением контракта)
• ОАК (RBC, HGB, HCT, MCV, MCH, MCHC, RDW + ретикулоциты, PLT)
• Коагулограмма (Фг, Пр, Ат111, ТВ. АЧТВ, РКМФ, Д-димер, ФА)
• БАК (мочевина, мочевая кислота, холестерин, липиды, глюкоза, АСТ, АЛТ, креатинин, КФК, КФК MB, ЩФ, ЛДГ, магний, кальций, фосфор, калий, натрий, железо, ферритин, амилаза, белок, альбумин, глобулин и фракции, аминокислоты, СМП, Тропонин –Т, BNP)
• Гормоны (кортизол, тестостерон, инсулин, С-пептид, адреналин, эритропоэтин, гормон роста , Соматомедин С, паратгормон, кальцитонин, ТТГ, св. Т4)
• Инфекции (TORCH, ЗППП)
• Наркотики
• Микроэлементы (цинк, хром, селен)
• Паразитологические обследования
• Пищевая непереносимость.
• Аллергия
• Микроэлементы
• КФК, ЛДГ, АСТ (умеренное повышение – результат недостаточности кровоснабжения мышц и перенапряжение скелетной мускулатуры при интенсивных занятиях, резкое повышение – недостаточная тренированность)
• КФК – МВ (повышение при поражении сердечной мышцы)
• Миоглобин (концентрация в крови пропорциональна мышечной массе. Отражает уровень подготовки атлета – выход в сыворотку миоглобина задерживается у тренированных спортсменов и увеличен у потерявших спортивную форму. Количество миоглобина в крови зависит от объема выполненной физической нагрузки, а также от степени тренированности спортсмена.)
• Тропонин (диагностика инфаркта миокарда)
• BNP (повышается при хронической сердечной недостаточности)
• (Na, K, Cl, Ca++, Mg) (нарушение водно-электролитного баланса, передачи нервного импульса, мышечного сокращения)
• Лактат и КОС (газы крови) (интенсивная работа скелетных мышц (особенно в начале занятий у нетренированных лиц или после длительного перерыва) сопровождается накоплением молочной кислоты и ацидозом)
• Гемоглобин и гематокрит (интенсивность эритропоэза и аэробного окисления)
• Гаптоглобин и билирубин (интенсивность гемолиза эритроцитов)
• ОАМ (рН, плотность, кетоны, соли, белок, глюкоза)
Спектр биохимических маркеров, позволяющих оценить влияние ФН на организм футболиста.
Маркеры контролирующие объем ФН
• ОАК (гемоглобин, гематокрит, эритроциты, лейкоциты)
• Биохимические показатели (мочевина, аммиак, холестерин, триглицериды, КФК, ферритин, железо, магний, калий, белок)
• Гормоны (кортизол, адреналин, дофамин, АКТГ, СТГ, Т3, инсулин, тестостерон) (повышение адренокортикотропного гормона, соматотропного гормона, кортизола, тестостерона и трийодтиронина, снижение содержания инсулина. При длительной ФН концентрации кортизола и индекса тестостерон/кортизол снижается).
• ОАМ (по наличию определенной концентрации белка в моче после выполнения физической работы судят о ее мощности. Так, при работе в зоне большой мощности она составляет 0,5 %, при работе в зоне субмаксимальной мощности может достигать 1,5 %).
Маркеры, контролирующие интенсивность ФН.
• ОАК (гемоглобин, гематокрит, эритроциты, ретикулоциты)
• Биохимические показатели (мочевина, аммиак, молочная кислота, мочевая кислота, холестерин, триглицериды, КФК, ЛДГ, АСТ, миоглобин, ферритин, трансферин, железо, магний, калий, общий белок и белковые фракции, СМП), КОС
• Гормоны (кортизол, тестостерон, Т/К, норадреналин, дофамин, эритропоэтин)
• ОАМ (рН, плотность, белок, кетоны)
• БАМ (креатин, креатинин в моче, кетоновые тела)
Маркеры перенапряжения и тренированности.
О более высоком уровне тренированности свидетельствуют
• Меньшее накопление лактата (по сравнению с нетренированными) при выполнении стандартной нагрузки, что связано с увеличением доли аэробных механизмов в энергообеспечении этой работы.
• Меньшее увеличение содержания лактата в крови при возрастании мощности работы.
• Увеличение скорости утилирации лактата в период восстановления после ФН.
• С увеличением уровня тренированности спортсменов увеличивается общая масса крови, что приводит к увеличению концентрации гемоглобина до 160—180 г • л»1 — у мужчин и до 130—150 г • л»1 — у женщин.
• Уровень саркоплазматических ферментов (КФК) и (ЛДГ) (повышение активности отражает значительное изменение проницаемости мембранных структур миоцита и адаптацию организма к ФН высокой интенсивности. Если у нетренированного человека при повреждении скелетной мускулатуры уровни КФК и ЛДГ растут на порядок, то у спортсменов они, часто остаются неизменными).
• Концентрация миоглобина и малондиальдегида (величина повышения активности КФК, миоглобина и уровня малондиальдегида отражают степень перенапряжение и деструкции мышечной ткани )
• БАМ (обнаружение креатина и 3-метил-гистидина, специфического метаболита мышечных белков, используется как тест для выявления перетренировки и патологических изменений в мышцах,)
• Магний, калий в крови (сниженная концентрация обнаружена у людей после неадекватной ФН и является следствием перетренировки и утомления – потеря с потом!!!)
• Хром (при недостаточности хрома в организме у футболистов нарушаются процессы высшей нервной деятельности, появляется беспокойство, утомляемость, бессонница, головные боли).
Маркеры утомления.
Мышечная утомляемость — неспособность мышц поддерживать мышечное сокращение заданной интенсивности — связана с избытком аммиака, лактата, креатинфосфата, недостатком белка
• Коэффициент восстановления:
— углеводного обмена (скорость утилизации молочной кислоты во время отдыха),
— липидного обмена (нарастание содержания жирных кислот и кетоновых тел в крови, которые в период отдыха являются главным субстратом аэробного окисления),
— белкового обмена (скорость нормализации мочевины при оценке переносимости спортсменом тренировочных и соревновательных физических нагрузок, хода тренировочных занятий и процессов восстановления организма). Если содержание мочевины на следующее утро остается выше нормы, то это свидетельствует о недовосстановлении организма либо развитии его утомления).
• Коэффициент микроциркуляции (КМ)=7,546Фг-0,039Tr -0,381АПТВ+0,234ФА+0,321РФМК-0,664ATIII+101,064 (должен равняться календарному возрасту)
• Определение содержания продуктов перекисного окисления в крови малонового диальдегида, диеновых конъюгатов. Биохимический контроль реакции организма на физическую нагрузку, оценка специальной подготов-ленности спортсмена, выявления глубины биодеструктивных процессов при развитии стресс-синдрома
• активность ферментов глутатионпероксидазы, глутатионредуктазы и каталазы, супероксиддисмутазы.
• Определение молекул средней массы (МСМ) (перекисное повреждение белковых веществ приводит к их деградации и образованию токсических фрагментов молекул средней массы, которые принято считать маркерами эндогенной интоксикации у спортсменов после интенсивной ФН. На ранних стадиях утомления уровень СМП возрастает по сравнению с нормой в среднем на 20-30 %, на средней стадии — на 100-200 %, поздних — на 300-400 %. )
• Коэффициент эндогенной интоксикации = СМП/ЭКА* 1000 (эффективная концентрация альбумина)
• ОМГ- тест (привлечение в очаг повреждения лейкоцитов которые в следствие активации выделяют большое количество активных форм кислорода тем самым разрушая здоровые ткани. Через одни сутки после интенсивной физической нагрузки активность гранулоцитов крови выше контрольного значения примерно в 7 раз и на этом уровне сохраняется в течение последующих 3 суток, затем начинает снижаться, превышая, однако, контрольный уровень и через 7 суток восстановления)
Маркеры повреждения мышечной ткани.
• Уровень саркоплазматических ферментов (КФК) и (ЛДГ)
• Миоглобин, тропонин, BNP
• Определение содержания продуктов перекисного окисления в крови малонового диальдегида, диеновых конъюгатов
• Активность ферментов глутатионпероксидазы, глутатионредуктазы и каталазы, супероксиддисмутазы
• Уровень активных форм кислорода (ОМГ- тест)
• БАМ (обнаружение креатина и 3-метил-гистидина)
Маркеры восстановления организма после ФН.
Восстановление организма связано с возобновлением количества израсходованных во время работы энергетических субстратов и других веществ. Уровень биохимических маркеров изучается на 1, 3, 7 день после интенсивной физической нагрузки.
• Уровень глюкозы.
• Уровень инсулина, кортизола.
• Скорость восстановления уровня молочной кислоты (лактата)
• Скорость восстановления уровня ферментов ЛДГ, КФК,
• Скорость восстановления уровня мочевины,
• Нарастание содержания свободных жирных кислот
• Снижение уровня малонового диальдегида, диеновых конъюгатов
• Общего белка и белковых фракций
• Восстановление до исходного уровня измененных показателй.
Кандидат медицинских наук, доцент
Б. А. Никулин.


ТЕЛЕФОНЫ ДЛЯ СПРАВОК
+7 499 967-8698
+7 965 237-0310
- TOP 50 АНАЛИЗОВ

Забор анализов на дому или в офисе
- Заболевания печени
- Инфаркт миокарда
- Госпитализация в хирургический стационар
Басогена 5е Актив — базовые минералы для регулирования кислотно-щеловного равновесия в удобной форме стика.
Известно, что чем более кислая среда в организме, тем выше риски, связанные со здоровьем. Поэтому важно контролировать уровень базовых щелочных минералов. Формула Басогена® 5е Актив содержит специально отобранные щелочные минеральные соединения в биодоступной форме и способствует восстановлению оптимального уровня pH при физических нагрузках.
Щелочное питание и спорт
Другая обзорная публикация детально исследует тренд как улучшить результаты в спорте с помощью щелочной диеты. При интенсивных тренировках возможны краткосрочные снижения pH в сторону кислот. При этом может снижаться результативность тренировок, чаще возникать утомление. 10 исследований, вошедших в обзор, подтверждают, щелочная диета может улучшить результаты даже при максимальной нагрузке. Авторы были бы рады увидеть дальнейшие исследования по этой теме, поскольку немногие доступные им исследования проводились лишь с помощью эргометров или беговых дорожек, а испытуемые были преимущественно мужского пола. Тем не менее в исследовании делается вывод, что диета с высоким содержанием щелочей может быть рекомендована людям любого возраста, занимающимся спортом, поскольку щелочные продукты (прежде всего фрукты и овощи, богаты витаминами, минералами, клетчаткой) в любом случае полезны для общего здоровья.
Ацидоз: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Ацидоз – это смещение кислотно-щелочного баланса организма в сторону повышения кислотности.
Кислотами называют вещества, способные отдавать ион водорода (Н+), а основаниями – вещества, способные его принимать. Кислоты постоянно образуются в результате жизнедеятельности клеток организма и расщепляются с освобождением очень активных ионов водорода.
Для поддержания нормальной жизнедеятельности организма концентрация этих ионов должна поддерживаться в физиологических значениях, этой цели служат буферные и выделительные системы организма (легкие, почки, кишечник).
Так поддерживается кислотно-щелочное равновесие (баланс) – относительное постоянство концентрации водородных ионов во внутренних средах организма.
Соотношение положительно заряженных ионов водорода (Н+) и отрицательно заряженных гидроксильных ионов (ОН-) во внутренней среде организма определяет интенсивность окислительно-восстановительных процессов, синтез и расщепление белков, жиров и углеводов, активность ферментов, проницаемость мембран, чувствительность к гормональным стимулам и др. Это соотношение определяется показателем рН (водородным показателем). Кислотность или щёлочность раствора зависят от содержания в нем свободных ионов водорода и концентрации гидроксильных групп. Если концентрация Н+ больше концентрации ОН-, то мы говорим о том, что среда кислая. Если концентрация Н+ равна концентрации ОН-, то среда нейтральная, когда концентрация Н+ меньше концентрации ОН-, то это щелочная среда. Таким образом, при рН < 7,0 среда кислая, при рН = 7,0 – нейтральная, рН ˃ 7,0 свидетельствует о щелочной среде.
В физиологических условиях показатель рН крови колеблется в пределах 7,35-7,45. Даже незначительные нарушения этих границ могут иметь неприятные последствия, а рН менее 6,8 и выше 7,8 несовместимы с жизнью.
Ведущую роль в поддержании кислотно-щелочного баланса крови играют буферные системы организма – растворы химических композиций, которые способны сглаживать изменения рН. Буфер состоит из основания и какой-нибудь слабой кислоты (слабыми считаются те кислоты, которые отдают не все ионы Н+ в раствор). Буферные системы крови – это первая «линия охраны», которая поддерживает рН при поступлении в кровь кислых или щелочных продуктов, пока те не будут выведены или использованы в метаболических процессах. Основные буферные системы организма – бикарбонатная, фосфатная, белковая и гемоглобиновая.
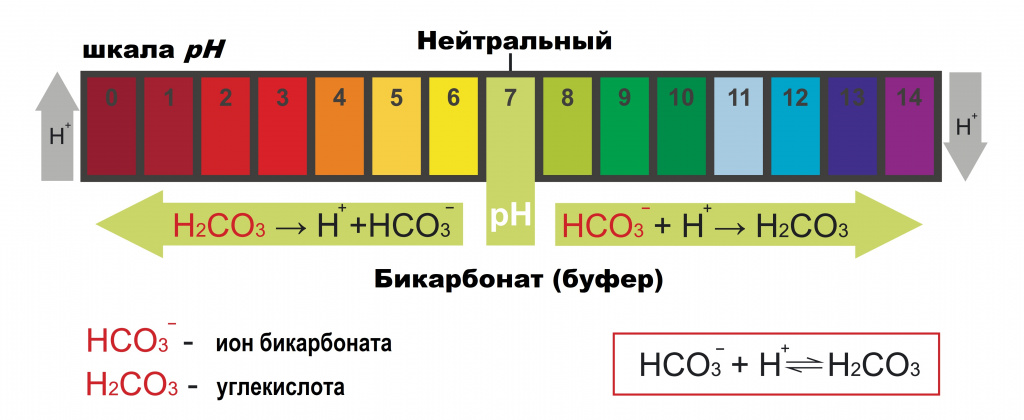
Наряду с химическими буферными системами действуют органные механизмы компенсации – легкие, почки, желудочно-кишечный тракт. Для достижения эффекта им необходимо больше времени – от нескольких минут до нескольких часов. Так, например, легкие обеспечивают устранение или уменьшение сдвигов кислотно-щелочного равновесия путем изменения объема альвеолярной вентиляции в течение нескольких минут (увеличение вентиляции легких в 2 раза повышает рН крови примерно на 0,2, снижение вентиляции на 25% может уменьшить рН на 0,3-0,4). Почки могут увеличивать выведение (экскрецию) ионов Н+ и восстанавливать резерв гидрокарбонатной буферной системы крови. В печени осуществляется синтез белков крови, входящих в белковую буферную систему, образуется аммиак, способный нейтрализовать кислоты, а молочная кислота, которую многие органы и ткани не способны метаболизировать, превращается в нейтральные продукты и т.д.
Если буферные системы не справляются, происходит нарушение баланса. В зависимости от направленности сдвига рН крови выделяют ацидоз и алкалоз.
Смещение рН менее 7,35 – ацидоз, смещение рН более 7,45 – алкалоз.
К симптомам ацидоза относят тошноту и рвоту, диарею, частое дыхание, головную боль, головокружение, нарушение сознания вплоть до комы, падение артериального давления, нарушения ритма сердца (от экстрасистолии до фибрилляции желудочков). Характерным признаком тяжелого метаболического ацидоза является медленное глубокое шумное дыхание или дыхание Куссмауля. Это симптом обычно наблюдается у пациентов в предтерминальном состоянии.
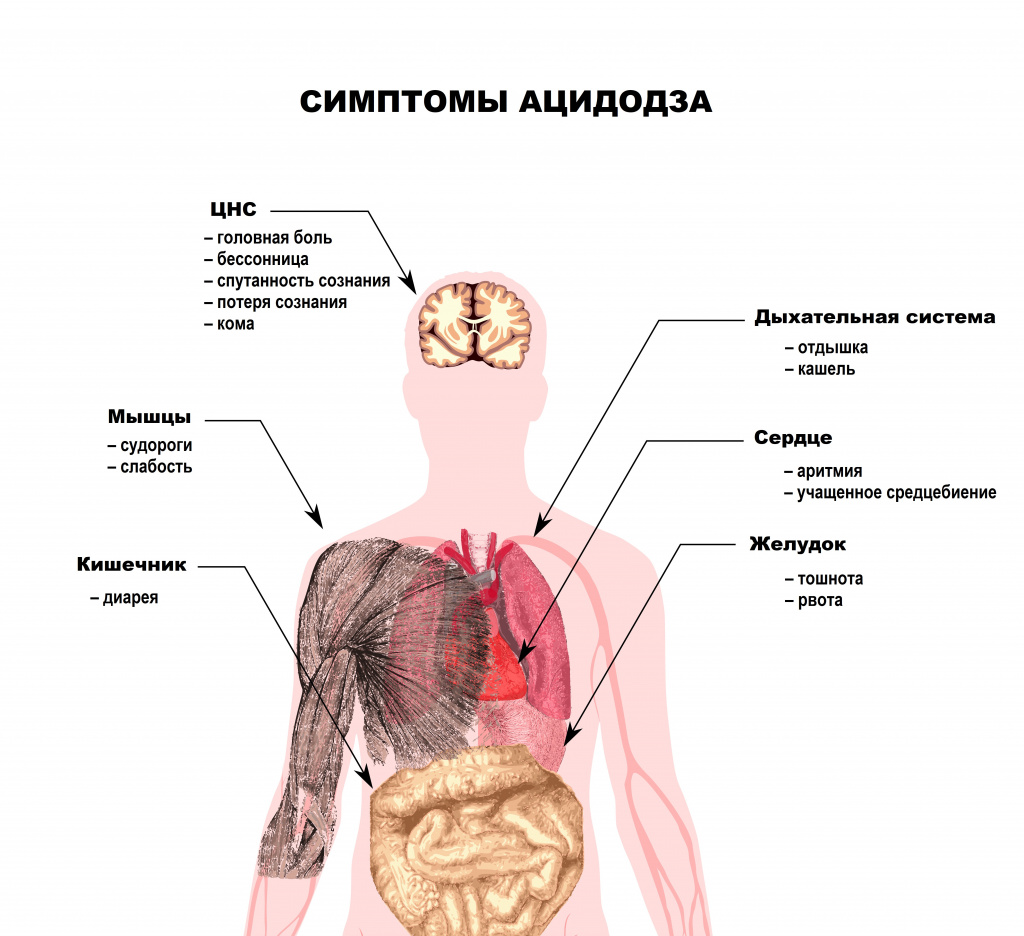
По механизму развития нарушения кислотно-щелочного равновесия выделяют респираторный, метаболический и смешанный ацидоз, а по степени компенсации – компенсированный, субкомпенсированный и декомпенсированный.
Компенсированными считаются такие сдвиги, при которых рН капиллярной крови не отклоняется за пределы диапазона нормы – 7,35-7,45, но присутствуют изменения других показателей. При рН 7,3-7,26 ставится диагноз «субкомпенсированный ацидоз», а при рН от 7,18 до 6,8 – «декомпенсированный ацидоз».
Возможные причины ацидоза
Причиной развития ацидоза могут быть как эндогенные факторы (заболевания, нарушения работы физиологических систем поддержания равновесия), так и экзогенные (связанные с избыточным поступлением в организм веществ кислого характера – лекарств, токсичных средств, некоторых продуктов питания).
В основе респираторного ацидоза лежит гиповентиляция, в результате которой в организме накапливается избыток CO2, а в последующем – углекислоты. Респираторный ацидоз может стать следствием обструкции (закупорки) дыхательных путей, нарушения растяжимости легких, нарушения регуляции дыхания, повышенного образования углекислого газа или его избыточного поступления в организм с вдыхаемым воздухом (при работе в скафандре, на подводных лодках) или при нахождении большого количества людей в замкнутом пространстве (например, в шахте).
Метаболический ацидоз развивается в результате повышенной продукции кислот, сниженной экскреции (выведения) кислот и/или повышенной экскреции оснований. Причинами метаболического ацидоза являются гипоксия, нарушение кровообращения, голодание, сахарный диабет, тяжелые поражения печени и почек, длительная интенсивная физическая нагрузка, ожоги, воспаление, травма, кровопотеря, гипопротеинемия. Бикарбонат (буфер) выделяется в полость тонкого кишечника для осуществления пищеварения и обратно всасывается в нижних отделах желудочно-кишечного тракта или выводится с фекалиями. Любые патологии пищеварительного тракта (например, тяжелая диарея) могут привести выведению бикарбоната из организма в количествах, достаточных для развития метаболического ацидоза. Также потеря бикарбонатов может быть связана с почечной недостаточностью. Тяжелый метаболический ацидоз способен стать следствием всасывания случайно попавших в пищеварительный тракт кислых соединений (например, метанола).
Заболевания, при которых может развиться ацидоз
Наиболее частые причины респираторного ацидоза — бронхиальная астма, бронхит, эмфизема легких, аспирация инородного тела, пневмония, гемоторакс, ателектаз легкого, инфаркт легкого, парез диафрагмы. Энцефалиты, полиомиелит, расстройства мозгового кровообращения могут стать причиной нарушения регуляции дыхания. Повышенное образование эндогенного CO2 является следствием лихорадки, сепсиса, длительных судорог, может сопровождать тепловой удар.
Распространенной причиной метаболического ацидоза является тяжелая диарея, при которой большое количество ионов бикарбонатов выводится с фекалиями. Эта форма метаболического ацидоза особенно опасна, поскольку способна приводить к летальному исходу, особенно у детей в раннем возрасте.
Канальцевый ацидоз возникает при хронической почечной недостаточности, недостаточной секреции альдостерона (болезни Аддисона), других наследственных и приобретенных заболеваниях, которые нарушают функцию почечных канальцев.
При значительном нарушении функции почек снижается выделение кислот с мочой и снижается образование ионов бикарбонатов, что тоже может привести к метаболическому ацидозу.
Усиленная продукция кетокислот является одной из особенностей неконтролируемого или плохо контролируемого инсулинозависимого сахарного диабета (диабетический кетоацидоз).
К каким врачам обращаться при ацидозе
Острые нарушения кислотно-щелочного равновесия являются жизнеугрожающими состояниями, поэтому пациенты госпитализируются в стационар под наблюдение врача-реаниматолога. В случае хронического ацидоза необходима коррекция основного заболевания (например, заболевания легких или почек), поэтому наблюдение осуществляет
врач-терапевт
или
врач-пульмонолог
,
кардиолог
, нефролог,
невролог
,
гастроэнтеролог
.
Диагностика и обследования при ацидозе
Диагноз устанавливается на основании оценки содержания электролитов и газов крови. Для исследования кислотно-щелочного состояния используются специальные автоматические анализаторы.
Измеряются такие показатели как:
- pH – концентрация ионов (активность) H+,
- рCO2 – парциальное давление CO2 (в мм рт.ст.),
- рO2 – парциальное давление O2 (в мм рт.ст.).
Рассчитываются показатели:
- HCO3 – концентрация бикарбоната (в ммоль/л),
- BE – избыток (или дефицит) оснований (в ммоль/л),
- BB – сумма оснований всех буферных систем крови (в ммоль/л),
- SBE – стандартный избыток оснований (в ммоль/л),
- SBC – стандартный бикарбонат (в ммоль/л).
При подозрении на диабетический, алкогольный кетоацидоз или связанный с голоданием кетоацидоз определяют содержание кетоновых тел при помощи нитропруссидного теста.
Необходимо также выполнить определенные исследования крови и мочи:
- общий анализ крови;
Что делать при ацидозе
При подозрении на ацидоз необходимо обратиться как можно быстрее за медицинской помощью.
Лечение ацидоза
Лечение ацидоза зависит от вызвавшей его причины, механизма развития, степени компенсации. Поэтому главная задача – устранение причины его развития, то есть терапия основного заболевания.
Для коррекции метаболического ацидоза могут применяться внутривенные инфузии натрия бикарбоната, препараты калия, в случае кетоацидоза на фоне сахарного диабета проводят инсулинотерапию. Острый респираторный ацидоз представляет угрозу для жизни пациента, поэтому требуется незамедлительное восстановление адекватной вентиляции легких и уровня оксигенации крови.
Источники:
- Тепаев Р.Ф., Ластовка В.А., Пыталь А.В., Савлук Ю.В. Метаболический ацидоз: диагностика и лечение // Педиатрическая фармакология. – 2016. – Т. 13. – № 4. – С. 384-389. DOI: 10.15690/pf.v13i4.1612
- Азбука кислотно-щелочного состояния: метод. указ. для врачей-интернов детских анестезиологов / сост. Межирова Н.М, Кравцова Г.Д, Данилова В.В., Коваль А.В., Овчаренко С.С. – Харьков, ХНМУ. – 2015.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.










